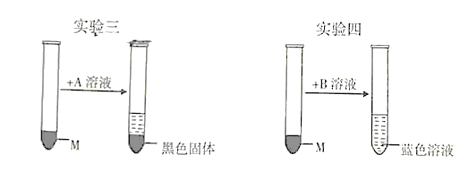
��Ŀ����
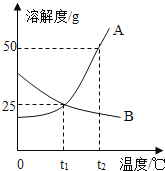
����Ŀ���±���NaCl�� KClO3�ڲ�ͬ�¶��µ��ܽ�ȣ���λ: g��
�¶ȣ���C�� | 0 | 20 | 40 | 60 | 80 | 100 |
S��NaC1�� | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
S��KClO3�� | 3.3 | 7.3 | 13.9 | 23.8 | 37.5 | 56.3 |
��1��20��Cʱ,NaCl���ܽ��Ϊ________��
��2��40��Cʱ,��10gKClO3����100gˮ�г���ܽ⣬������Һ������������Ϊ________������ȷ��0.1% ��
��3������ˮɹ�������õķ�����__________�������������ᾧ���������½ᾧ���� ;
��4��ʵ���ҿ����ü���һ���������������������̵Ļ������ȡ����,������Ҫ����9.6g������ֹͣ����,������Ӧ������ص�����Ϊ________g.��Ӧ��ʣ�����ijɷֿ���Ϊ________��
��5����ҵ�����Ȼ�����Һ�Ʊ������,��Ҫ��������:
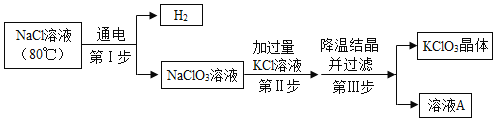
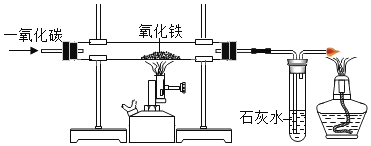
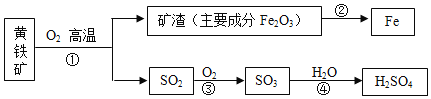
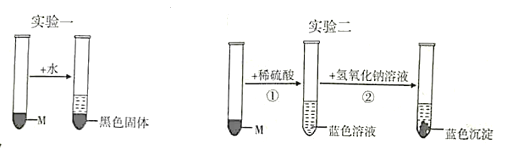
����II���з����ķ�Ӧ: ![]() ��
��
�ٵ�I����Ӧ�Ļ�ѧ����ʽΪ_________��
����ҺA�к��е�������__________���ѧʽ�� .
���𰸡�36.0g 9.1% �����ᾧ 24.5 ��KCl��MnO2��KClO3����KCl��MnO2 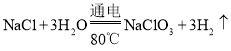 NaCl��KCl��KClO3
NaCl��KCl��KClO3
��������
��1�������֪��20��ʱ���Ȼ��Ƶ��ܽ��Ϊ36.0g���ʴ�Ϊ��36.0g��
��2��40��ʱ������ص��ܽ��Ϊ13.9g������40��ʱ��100g��ˮ�У�������ܽ�13.9g�����������Ϣ���ܽ�10g������أ����γɸ��¶��µ�����صIJ�������Һ����������������Ϊ��![]() ���ʴ�Ϊ��9.1%��
���ʴ�Ϊ��9.1%��
��3����ˮɹ�Σ����ܼ�ˮ�����������Ӷ��������塣�ù����������ᾧ���ʴ�Ϊ�������ᾧ��
��4��������9.6g������Ҫ����ص�����Ϊx��
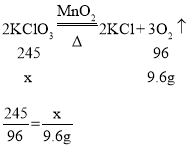
���x=24.5g�����������Ϣ��������ȡ9.6g������ֹͣ���ȣ�������ؿ���ǡ����ȫ��Ӧ��������ʣ�ࡣ��Ӧ��ʣ��Ĺ���һ�������ɵ��Ȼ��ء������������̣�����������ء��ʴ�Ϊ��24.5g����KCl��MnO2��KClO3����KCl��MnO2��
��5���ٸ��������غ㶨�ɿ�֪����ѧ��Ӧǰ��Ԫ�ص�����䡣��Ӧ������Ԫ�أ���ӦǰҲӦ������Ԫ�أ����Ʋ���Ԫ��������ˮ�����Ȼ��ƺ�ˮ��Ӧ���������������ơ��ʴ�Ϊ��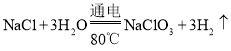 ��
��
��ͨ��������֪�����̢��м����˹�����KCl��Һ���ҷ�Ӧ�����Ȼ��ƣ�������ҺA�к���KCl��NaCl����Ϊ���½ᾧ��õ���A��ҺΪ����صı�����Һ��������ҺA��������ء��ʴ�Ϊ��NaCl��KCl��KClO3��

 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�����Ŀ�����ࡢ��ȡ���������ѧϰ��ѧ���õķ�����
��1�����ʵ����ʺܴ�̶��Ͼ��������ʵ���;����֪���ʵ����ʲ��ܸ��õ�Ӧ�����ʣ���ͼΪ���л�ѧ�̲��е�ʵ�顣��ش����⣺
A�� | B�� | ʵ��C | ||
ʯī����ʵ�� |
������̼���ܽ���ʵ�� |
����ȼ�� |
��ʯ���м���ˮ |
�������Һ�ı仨����ɫ |
�������о��������ʵĽǶȽ��з��࣬Ӧ��ʵ��C��Ϊ_____�飬������_____��
��2��ͨ�������Ķ����������з�Ӧ��
Cl2+2NaBr=2NaCl+Br2 Br2+2KI=2KBr+I2
Cl2 Br2 I2 ���ȡ��塢������Ԫ����ɵ����ַǽ������ʡ�������ȷ��������ַǽ����������η������û���Ӧ���������η������û���Ӧ�����ƵĹ��ɡ���˿����ж�Cl2 Br2 I2 ���ַǽ����л�������ǿ����_____��д��ѧʽ����
���������ֵ�֪���ۣ���Ļ����Ա��������ֵ��ʵĻ����Զ����������������Ӧ������Ԫ�غͼ�Ԫ����ɵĻ��������䷢����һ����Ӧ��֤���˽��ۣ��û�ѧ����ʽ�ش�_____��