题目内容
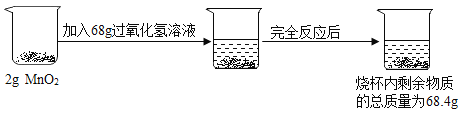
【题目】黑色粉末A和无色液体B混合,生成一种无色无味的气体C;加热暗紫色固体E,可同时得到A和C;气体C能使带火星的木条复燃。若加热某白色固体D与A的混合物可得到C和另一种物质F。
(1)写出上述物质的化学符号:C_____、F____
(2)写出D和A反应的文字表达式____,反应的基本反应类型为______反应。
【答案】O2 KCl 氯酸钾![]() 氯化钾+氧气 分解
氯化钾+氧气 分解
【解析】
无色气体C能使带火星的木条复燃,所以C是氧气,加热暗紫色固体E,可同时得到A和氧气,所以E是高锰酸钾,将黑色粉末A和无色液体B混合,生成氧气,所以A是二氧化锰,B是过氧化氢溶液,将加热某白色固体D与A的混合物可得到氧气,所以D是氯酸钾,F是氯化钾,经过验证,推导正确。
(1)C是O2;F是KCl;
(2)D和A是加热氯酸钾和二氧化锰生成氯化钾和氧气,反应的文字表达式氯酸钾![]() 氯化钾+氧气,此反应属于分解反应。
氯化钾+氧气,此反应属于分解反应。

【题目】当把燃着的小蜡烛放入一个集气瓶中并塞紧胶塞时,蜡烛一会儿就熄灭了。那么,蜡烛为什么会熄灭呢?某化学兴趣小组进行了如下探究,请你填答相关空格。
[提出猜想]
猜想I:蜡烛燃烧把集气瓶内的氧气耗尽,导致蜡烛熄灭。
猜想II:蜡烛燃烧随集气瓶内氧气含量降低而变弱,放出的热量减少,使温度降至蜡烛的着火点以下,导致蜡烛熄灭。
猜想III:蜡烛燃烧产生的二氧化碳能灭火,导致蜡烛熄灭。
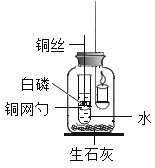
[进行实验]小组设计如下图所示的实验装置,并进行实验来验证猜想。
| 实验操作 | 实验现象 |
点燃蜡烛并连同胶塞上的其它仪器药品一起放入集气瓶中,塞紧胶塞。 | 蜡烛火焰逐渐变微弱最终_________ | |
蜡烛熄灭并静置冷却后,将铜丝上提,使盛白磷的铜网勺高于试管口,试管倒下,水流出。 | 一会儿后,白磷着火燃烧,有大量______________产生。 |
[分析及结论]
(1)蜡烛熄灭前,要让白磷浸没在小试管所盛的水中,目的是_______。
(2)生石灰遇水发生化学反应放出大量的热,集气瓶中装入一些生石灰的设计,目的是让它发生反应提高瓶内的_______,写出生石灰与水反应的方程式_________。
(3)瓶内的白磷能燃烧,证明猜想________和_________不能成立。我们根据成立的猜想认为,应该把“燃烧需要氧气”这一燃烧发生的条件补充完善为“_______”。
【题目】下表是Na2CO3、NaCl的溶解度。依据表中数据和实验完成下面小题。
温度 | Na2CO3 | NaCl |
20℃ | 21.8g | 36.0g |
30℃ | 39.7g | 36.3g |
20℃时,向2只盛有100g水的烧杯中,分别加入30g两种固体,充分溶解。

【1】上述溶液为饱和溶液的是( )
A.①B.②C.③D.④
【2】下列说法正确的是( )
A.①所得溶液中溶质与溶剂质量比为3:10
B.②所得溶液中溶质的质量分数为30%
C.①和③的溶质质量分数相等
D.③和④的溶质质量分数相等