题目内容
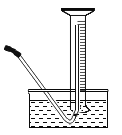
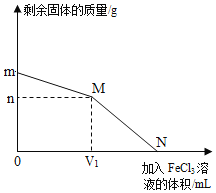
【题目】将铜粉和铁粉的混合物mg放入烧杯中,向烧杯中不断加入FeCl3溶液,测得烧杯中剩余固体的质量与加入FeCl3溶液体积的关系如图所示。已知:铁和铜都能与FeCl3溶液发生反应,有关化学方程式为:①Fe+2FeCl3=3FeCl2 ②Cu+2FeCl3=CuCl2+2FeCl2.下列说法正确的是( )
A.FeCl3与Cu发生的反应属于置换反应
B.M点溶液中一定含有FeCl2和CuCl2
C.加入V1mLFeCl3,溶液时,Fe恰好完全反应
D.混合物中铁粉与铜粉的质量比为m:n
【答案】C
【解析】
在金属活动性顺序中,铁在铜的前面,铁能与铜盐溶液发生置换反应,向装有氯化铁溶液的烧杯中,加入一定量的Cu和Fe的混合粉末,则铁优先与氯化铁发生反应生成氯化亚铁,然后铜与氯化铁反应生成氯化铜和氯化亚铁。
A、FeCl3与Cu发生的化学反应,由两种物质生成了一种物质,属于化合反应,不是置换反应,故 A错误。
B、根据反应特点,铁金属活动性强于铜,所以是铁与氯化铁先反应,铁的相对分子质量小于铜的相对分子质量,因此铁与氯化铁质量减少幅度不如铜与氯化铁反应的大,故在M点时是铁正好与氯化铁反应完毕,此时溶液中不含有铜离子,故B错误。
C、当加入V1mLFeCl3溶液时,铁恰好完全反应,故C正确。
D、在M点时,铁全部反应,剩余固体全部为铜,所以铜质量ng,铜粉和铁粉的混合物mg,铁粉的质量为(m-n)g,铁粉与铜粉的质量比为(m-n):n,故D错误。
故选:C。

【题目】下列归纳总结完全正确的一组是( )
A.分子的特征 | B.数字“2”的含义 |
①水分子很小 ②固体物质的分子不运动 ③气体分子间的间隔很大 | ①Fe2+:1个亚铁离子带2个单位正电荷 ② ③NO2:1个二氧化氮分子中含有2个原子 |
C. 生活经验 | D.节约资源 |
①常用钢刷擦洗铝制品 ②食品包装中抽真空防腐 ③用汽油洗去衣服上的油污 | ①提倡使用太阳能 ②回收利用废旧金属 ③农业灌溉采用滴灌 |
A.AB.BC.CD.D