题目内容
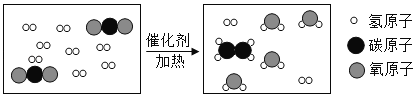
【题目】如图为铜-锌-稀硫酸构成的原电池示意图,下列说法错误的是

A.该装置能将化学能转变为电能
B.反应实质是锌原子失去电子,氢离子得到电子,电子的定向移动形成电流
C.电子由铜片通过导线流向锌片
D.锌片为负极,且锌片逐渐溶解,铜片为正极,且铜片上有气泡
【答案】C
【解析】
A、原电池装置是将化学能转化为电能的装置,故A正确
B、反应实质是锌原子失去电子,氢离子得到电子,电子的定向移动形成电流,故B正确;
C、原电池中电流从正极流向负极,即从铜片经导线流向锌片,而电子运动的方向正好与之相反,故C错误;
D、Zn、Cu、硫酸构成的原电池中,活泼金属锌做负极,所以铜为原电池的正极,氢离子在铜极上得电子生成氢气,所以铜片上有气泡产生,故D正确。故选C。

练习册系列答案
相关题目
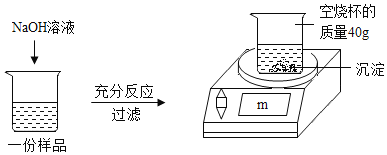
【题目】为测定某CuSO4溶液中溶质的质量分数,取150g CuSO4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见下表。请计算:
实验1 | 实验2 | 实验3 | |
样品质量/g | 50 | 50 | 50 |
NaOH溶液质量/g | 20 | 40 | 60 |
m/g | 42.45 | 44.9 | 44.9 |
(1)50g CuSO4溶液完全反应时,所得沉淀的质星为_____g。
(2)CuSO4溶液中溶质的质量分数为_____。