题目内容
【题目】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。
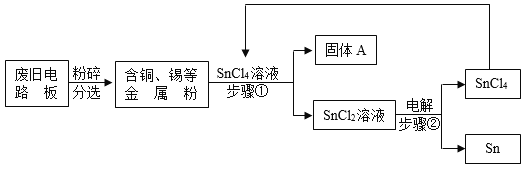
已知:Sn+SnCl4=2SnCl2
(1)废旧电路板粉碎为粉末在步骤①中的作用是_______。
(2)步骤①中进行的操作是______,固体A中一定含有的金属元素是_____。
(3)写出步骤②发生反应的化学方程式______。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是_______(回答一点即可)。
【答案】增大反应物接触面积,加快反应速率 过滤 铜 2SnCl2![]() Sn+SnCl4 避免了塑料燃烧产生污染环境的物质
Sn+SnCl4 避免了塑料燃烧产生污染环境的物质
【解析】
(1)废旧电路板粉碎为粉末在步骤①中的作用是增大反应物接触面积,加快反应速率;
(2)步骤①中进行的操作是过滤,通过过滤把液体和固体分离,在金属活动顺序中,铜排在锡之后,不能与SnCl2反应,固体A中一定含有的金属元素是铜;
(3)步骤②中,通电条件下SnCl2分解生成Sn、SnCl4,发生反应的化学方程式:2SnCl2![]() Sn+SnCl4;
Sn+SnCl4;
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是避免了塑料燃烧产生污染环境的物质。

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案
相关题目