��Ŀ����
����Ŀ����1������ʵ����õ�ˮ������ˮ����Ϊ�ܼ�����_____������ĸ��ţ���
A ����0.9%��������ˮ B ��ʯ�ұ����ʯ�� C Ũ����ϡ��
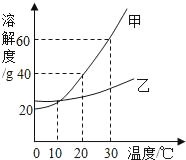
��2����ͼΪKNO3��NaCl�������ʵ��ܽ�����ߡ�
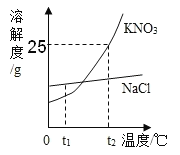
�����������ܽ�ȵı仯���¶�Ӱ��ϴ����_________�� t1��ʱ�����������ܽ�ȵĴ�С��ϵ��NaCl_____ KNO3������>������=������<������
��t2��ʱ����15g KNO3����Ͷ��50gˮ�У�����ܽ��ɵõ� KNO3________��Һ������������������������������ʱ��Һ��KNO3������������__________��
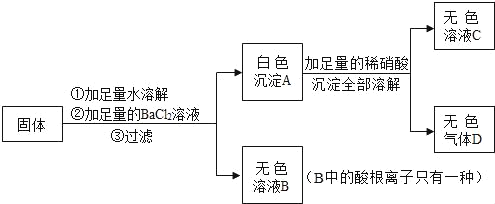
��3����ҵ�Ͻ�����غ��Ȼ��Ƶ��Ȼ����Һ�����߾��Ѵﱥ�ͣ���ȴ�����£��������塣�������ľ����ʣ����Һ������ȷ����__________����д��ĸ����
A ʣ����Һһ����KNO3������Һ B ʣ����Һһ����NaCl������Һ
C �����������Խ�������ȫ���� D �����ľ�����ֻ����KNO3
���𰸡�A��C KNO3 > ���� 20% A��B
��������
��1��A������0.9%��������ˮ���õ���ˮ��ˮ����Ϊ�ܼ�����Ϊ������ˮ����Һ���������ƹ������Ȼ��Ʋ���ˮ������Ӧ��B����ʯ�ұ����ʯ�ҹ����У���ʯ�Һ�ˮ��Ӧ������ʯ�ң�ˮ�Ƿ�Ӧ�C��Ũ����ϡ�����У�ˮ����Ϊ�ܼ�����Ϊ�ڴ˹����У�ˮû����Ũ���ᷢ����Ӧ����ϡ�ͳɵ�ϡ������ˮ���ܼ���������ʵ����õ�ˮ������ˮ����Ϊ�ܼ����ǣ�A��C��
��2���ٴ���Ŀ�ṩ���ܽ�������п�֪�����������ܽ�ȵı仯���¶�Ӱ��ϴ���ǣ�KNO3��t1��ʱ�����������ܽ�ȵĴ�С��ϵ��NaCl> KNO3��
����Ϊt2��ʱ��KNO3���ܽ����25g�����Խ�15g KNO3����Ͷ��50gˮ�У�����ܽ��ֻ���ܽ�12.5g��ʣ��2.5g���岻���ܽ⣬��˵õ�KNO3������Һ����ʱ��Һ��KNO3�����������ǣ�![]() ��
��
��3����ҵ�Ͻ�����غ��Ȼ��Ƶ��Ȼ����Һ�����߾��Ѵﱥ�ͣ���ȴ�����£��������塣��Ϊ����غ��Ȼ��Ƶ��ܽ�ȶ����¶Ƚ��Ͷ���С����������غ��Ȼ���ͬʱ���о���������������ص��ܽ�ȱ仯������������ؾ���࣬�Ȼ��Ƶ��ܽ�ȱ仯С���������Ȼ��ƾ����٣�ʣ�����Һ��������غ��Ȼ�����˵���DZ�����Һ�����ʣ����Һһ����KNO3������Һ��ʣ����ҺҲһ����NaCl������Һ��A��B��ȷ����Ϊ�ǽ�����غ��Ȼ��Ƶ��Ȼ����Һ�����߾��Ѵﱥ�ͣ���ȴ�����£��������壬����غ��Ȼ��Ƶ��ܽ�ȶ����¶Ƚ��Ͷ���С������غ��Ȼ���ͬʱ���о������������þ����мȺ��������Ҳ�����Ȼ��ƣ����������������ܽ�������ȫ���룬C����ȷ����Ϊ���þ����мȺ���������ֺ����Ȼ��ƣ�����D����ȷ����������ȷ���ǣ�A��B��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ������ʵ�鷽��һ���ܴﵽʵ��Ŀ�ĵ���
ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
A | ����һƿ�����Ƿ�Ϊ | ��ȼ�ŵ�ľ������ƿ�� |
B | ���� | �ֱ��ȼ���ڻ����Ϸ���һ�����ձ� |
C | ����ʯ��ˮ�� | ����������ϡ���� |
D | �Ƚ�Zn��Cu��Ag�Ľ������ | ��Zn��Ag�ֱ���� |
A. A B. B C. C D. D
����Ŀ��ijС��ͬѧ��þ����CuSO4��Һ��Ӧ��ʵ���У����˹۲쵽þ�����к�ɫ�������������۲쵽����ɫ��ζ�����������Һ���г������ɡ������ڲ������ϵĻ����ϣ��������ʵ�������һ����չ̽����

���������ϣ�
i. ������ͭ�ͼ�ʽ����ͭ[Cu2(OH)2SO4]��������ˮ������ҺpH < 2ʱ������ϡ���ᷢ�����·�Ӧ��
Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
Cu2 (OH)2SO4 + H2SO4 = 2CuSO4 + 2H2O
ii. þ��ͭ������Ũ���ᷴӦ��
Mg+4HNO3=Mg(NO3)2����ҺΪ��ɫ��+2NO2��������ɫ��+2H2O
Cu+4HNO3=Cu(NO3)2����ҺΪ��ɫ��+2NO2��������ɫ��+2H2O
��������裩
I��þ���ϵĺ�ɫ�����ǽ���ͭ��
II����ɫ��ζ������_____��
III����Һ�����ɵij���������������ͭ��Ҳ�����Ǽ�ʽ����ͭ����ߵĻ���
������ʵ�飩
��� | ʵ����� | ʵ���������� | ʵ����� |
1 | ȡ10 mL 10% CuSO4��Һ���Թ��У��ⶨ ��ҺpH | pH ԼΪ3.4 | ���� |
2 | ��ʵ��1�Թ��м���������ĥ������þ�� | ������ɫ��ζ���壬þ�����渽�ź�ɫ���ʣ���Һ�г��ֳ��� | |
3 | ��ʵ��2�еõ��ĸ��ź�ɫ���ʵ�þ�������Թ��У�����Ũ���� | _____ | ����I���� |
4 | ��С�Թ��ռ�ʵ��2�в��������壬��Ĵָ��ס���������С�Թܹܿڣ������ƾ��ƻ��棬�ƿ�Ĵָ | ����ı��������Թ��ڱ�����ɫҺ�� | ����II���� |
5 | �ظ�ʵ��2�����ˡ��ռ���Һ�еij��������ɣ����� | ���� | ���� |
6 | ȡ2֧�Թܣ��ֱ���Ϊ�Թܼ��Թ��ң����Թܼ��м���1 g_____�����Թ����м���1 g_____���ٷֱ���2֧�Թ��м���5 g���ʵ���������Ϊ10%��ϡ���� | �Թܼ��й���ȫ���ܽ⣬�Թ��������й���ʣ�� | �����Ǽ�ʽ����ͭ |
����������ۣ�
��1��þ��������ͭ�����û���Ӧ�Ļ�ѧ����ʽ��_____��
��2����ʵ��1�����֪��CuSO4��Һ��_____���������������������������ԡ�
��3��ʵ��3�У��۲쵽��������_____��
��4������ʵ��4��ȫ����II��_____��
��5���Թܼס��Թ����м�������ʷֱ���_____��_____������ĸ��ţ���
A ������ͭ B ʵ��5�еõ��Ĺ���
����˼�����ۣ�
��6����ͬѧ��Ϊ����ʵ��6���ݺ�����ó��������Ǽ�ʽ����ͭ�����۲���ȷ����ȷ�Ľ���ӦΪ_____��
����Ŀ��̼������(NaHCO3)�׳�С�մ�����ʳƷ��ҽҩ��ҵ��ij��ѧ��ȤС���ͬѧ��̼�����Ƶ����ʽ���������̽����
ʵ��һ��̽��̼��������Һ���������pH��ֽ���̼��������Һ��pH=10���ɴ˿�֪������̼��������Һ�еμ���ɫ��ʯ����Һʱ����Һ��_______ɫ��
ʵ�����̽��̼�����Ƶ����ȶ���
[��������]��̼�������������ֽ⣬����ˮ��������̼�����һ�������Ĺ������ʡ�
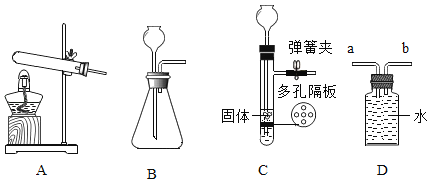
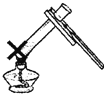
[����ʵ��]��Ϊ��֤̼����������ʱ��ֽ⣬��ȤС���ͬѧȡһ��������̼�����Ʒŵ�ͭƬ�ϼ��ȣ�����ͼ��ʾ��

(1)����һ��ʱ��۲쵽�ձ��ڱ���_______________��
(2)��ȤС���ͬѧ��Ϊ��ּ��Ⱥ�Ĺ�����������NaOH��Na2CO3��
�����Dz����������____________________________��
��Ϊ̽����Ӧ��Ĺ�����ﵽ����NaOH����Na2CO3�������ֽ��������±���ʵ�鲢�õ����ۣ���������±���
ʵ �� �� �� | ʵ������ | �� �� |
_______________ | ____________ | ���������Na2CO3 |