题目内容
【题目】(1)某同学对蜡烛(主要成分是石蜡)及其燃烧进行如下探究,请填写下列空格:(1)取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上。由此可推导石蜡的三个物理性质是___________,____________,_______________。
(2)点燃蜡烛,观察蜡烛火焰分为外焰、内焰、焰芯三层。把一根火柴放在蜡烛的火焰中,如图所示,约1s后取出,可以看到火柴梗的______(填“a”、“b”或“c”)处最先碳化。结论:蜡烛火焰的_________层温度最高。

(3)再将一只干燥的小烧杯罩在蜡烛的上方,烧杯内壁出现水雾;用另一只内壁被澄清石灰水润湿的烧杯罩在火焰上方,澄清石灰水变浑浊结论:说明蜡烛燃烧的生成物中含有_________和________。由此可证明石蜡中一定含有____________元素;
(4)在该实验中,将蜡烛熄灭,灯芯上有白烟冒出。探究:蜡烛刚熄灭时产生的白烟是什么?
提出问题:蜡烛刚熄灭时,总会有一缕白烟冒出,它的成分是什么?
提出假设:
A.白烟是燃烧时生成的二氧化碳
B.白烟是燃烧时生成的水蒸气
C.白烟是石蜡蒸气凝成的石蜡固体
实验探究:针对上述三个假设进行实验,①吹灭蜡烛,立即用一个沾有澄清石灰水的烧杯罩住白烟,其目的是为了验证假设________(填序号)。
②吹灭蜡烛,立即用一块干而冷的玻璃片放在白烟上,玻璃片上没有出现水雾,说明白烟不是_____________ 。
③吹灭蜡烛,立即用燃着的木条去点白烟。(注意不要接触烛芯),发现蜡烛重新被点燃,说明白烟具有可燃性,这为假设___________提供了证据。同时可排除假设___________,因为_________________。
【答案】 质软 不溶于水 密度比水小 a 外焰 水 二氧化碳 碳和氢 A 水蒸气 C AB 二氧化碳和水蒸气不能燃烧
【解析】(1)用小刀切下一小块,把它放入水中,蜡烛浮在水面上,据此判断石蜡质软、不溶于水、密度比水的密度小;
(2)蜡烛的火焰分为外焰、内焰、焰心三层;温度越高,木条碳化的越快,进行分析;
(3)从化学反应前后元素的种类不变进行分析;
(4) ①根据二氧化碳可使澄清石灰水变浑浊,从而判断是验证哪种假设,据此进行分析;
②熄灭蜡烛,并立即用一块干而冷的玻璃片放在白烟上,发现玻璃片上没有出现水雾,据此进行分析;
③熄灭蜡烛,并立即用燃着的木条伸到白烟处(不接触烛芯),发现蜡烛重新被点燃,这说明白烟具有可燃性,据此进行分析。
解:(1)取一支蜡烛,用小刀切下一小块,说明石蜡的硬度小;把它放入水中,蜡烛浮在水面上,说明石蜡不溶于水、密度比水的小;
(2)蜡烛的火焰分为外焰、内焰、焰心三层;把一根火柴梗放在蜡烛的火焰中约1s后取出,取出可以看到火柴梗的a处最先碳化,说明蜡烛火焰的外焰温度最高;
(3)根据质量守恒定律:化学反应前后元素的种类不变,将一只干燥的小烧杯罩在蜡烛的上方,烧杯内壁出现水雾;用另一只内壁被澄清石灰水润湿的烧杯罩在火焰上方,澄清石灰水变浑浊结论:说明蜡烛燃烧的生成物中含有水和二氧化碳。由此可证明石蜡中一定含有碳和氢元素;
(4) ①二氧化碳可使澄清石灰水变浑浊,熄灭蜡烛,并立即用一个沾有澄清石灰水的烧杯罩住白烟,其目的是为了验证假设A;
②吹灭蜡烛,立即用一块干而冷的玻璃片放在白烟上,玻璃片上没有水雾,说明白烟不是水蒸气;
③熄灭蜡烛,并立即用燃着的木条伸到白烟处(不接触烛芯),发现蜡烛重新被点燃,这说明白烟具有可燃性,这就证明了假设C正确;又因为水蒸气和二氧化碳都不能燃烧,所以同时可排除假设AB,因为水蒸气和二氧化碳都不能燃烧。

 名校课堂系列答案
名校课堂系列答案【题目】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(图1)。
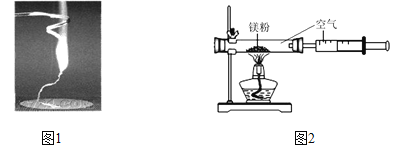
(1)请写出镁条与氧气反应的化学方程式___________________。
(2)小明认为根据质量守恒定律,燃烧产物的质量应大于反应物镁条的质量。镁条完全燃烧后,称量发现石棉网上的燃烧产物质量反而比反应前镁条质量小,其主要原因是 __________________________。
(3)小红按图2装置改进实验,验证了质量守恒定律,却发现产物中还有一些黄色固体。
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
【做出猜想】黄色固体为Mg3N2
【实验探究】
实验操作 | 实验现象及结论 |
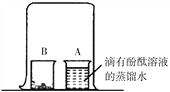
如图,取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B。
| 现象:_______________。 结论:燃烧产物中含Mg3N2 |
【反思与交流】
①为什么在发生化学反应前后各物质的质量总和相等?请从微观角度解释。
___________________________________________________。
②空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释____________________。
【拓展延伸】
①如果用图2装置(气密性良好)和药品(足量)测定空气中氧气含量,该实验所测得的氧气体积分数_____1/5(填“大于”、“小于”或“等于”)。
②2.40g镁条在某氧气和氮气的混合气中完全燃烧,所得固体质量可能是______。
A. 3.33g B. 4.00g C. 3.28g D. 3.96g