题目内容
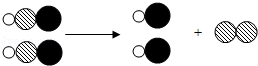
【题目】初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH﹣═H2O.如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式.离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例) 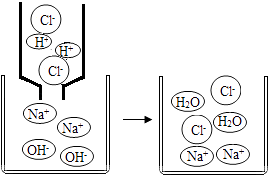
①写出Na2SO4与BaCl2反应的化学方程式: ;
②把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示.上述方程式可改写成:2Na++SO42﹣+Ba2++2Cl﹣═BaSO4↓+2Na++2Cl﹣
③删去方程式两边不参加反应的离子:Ba2++SO42﹣═BaSO4↓
④检查方程式两边各元素的原子个数和电荷总数是否相等.
请回答:
【答案】Na2SO4+BaCl2=BaSO4↓+2NaCl
(1)下列各组中的离子,在pH=3的水溶液中能大量共存的是。
A.Na+、Mg2+、Cl﹣、SO4 2﹣
B.Na+、K+、Cl﹣、OH﹣
C.Na+、Cu2+、Cl﹣、SO42﹣
D.Na+、K+、Cl﹣、CO32﹣
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式;
(3)写出一个与离子方程式Mg+2H+═Mg2++H2↑相对应的化学方程式;
(4)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或生成,反应就能发生.
【答案】
(1)AC
(2)CaCO3+2H+=Ca2++H2O+CO2↑
(3)Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑
(4)水
【解析】解:Na2SO4与BaCl2反应的化学方程式:Na2SO4+BaCl2=BaSO4↓+2NaCl;(1)A.这几种离子之间不反应,所以能大量共存,故正确;B、H+ 和OH﹣ 反应生水,故错误;
C、这几种离子之间不反应,所以能大量共存,故正确;
D.H+ 和 CO32﹣ 反应生成二氧化碳和水,故错误;(2)石灰石和盐酸反应的离子反应为:CaCO3+2H+=Ca2++H2O+CO2↑;故填:CaCO3+2H+=Ca2++H2O+CO2↑;(3)与离子方程式Mg+2H+=Mg2++H2↑相对应的化学方程式:Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑;故填:Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑.(4)复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,生成物中有气体或沉淀或水;反应就能发生.故填:水.
答案:Na2SO4+BaCl2=BaSO4↓+2NaCl(1)AC;(2)CaCO3+2H+=Ca2++H2O+CO2↑;(3)Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑.(4)水.
根据反应原理写出反应的化学方程式;(1)离子之间不反应生成气体、沉淀、弱电解质或络合物或发生氧化还原反应、双水解反应的就能共存,据此分析解答.(2)反应生成氯化钙、水、二氧化碳,水、二氧化碳、碳酸钙在离子反应中保留化学式;(2)反应生成KCl和碘,氯气、碘在离子反应中保留化学式.(3)非氧化性的强酸如稀硫酸、稀盐酸与金属镁的反应.(4)复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,生成物中有气体或沉淀或水;反应就能发生.

 中考解读考点精练系列答案
中考解读考点精练系列答案【题目】掌握科学的研究方法,探索化学世界的奥秘.
(1)分类是学习化学的重要方法之一. 生活中,常会接触到下列物质:A.铜丝 B.天然气 C.干冰 D.食盐水
其中属于混合物的是(填字母,下同),属于氧化物的是 .
(2)控制变量,设计对比实验是实验探究的重要方法.
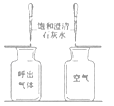
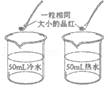
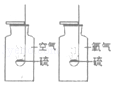
实验编号 | 1.探究人体呼出气体中二氧化碳含量比空气中的高 | 2、探究影响品红扩散快慢的因素 | 3、探究硫在空气和氧气中燃烧 |
实验设计 |
|
|
|
实验分析 | 本实验条件除了要控制两个盛装气体样品的集气瓶大小规格相同外,还要控制相同. | 发现两杯水都变红,且整杯热水变红时间比冷水要短,由此说明:①分子在不断运动;②影响分子运动快慢的因素有 . | 取等量的硫粉点燃后,分别插入相同规格的盛有空气和氧气样品的集气瓶中,发现硫在氧气中燃烧更剧烈,该对比实验所得结论为 . |
(3)质量守恒定律是帮助我们学习和认识化学反应实质的重要理论. ①下列表述正确的是 .
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32gS和32gO2完全反应后,生成64gSO2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②物质X是一种可再生绿色能源,其燃烧的化学方程式为X+3O2 ![]() 2CO2+3H2O,则X的化学式为 .
2CO2+3H2O,则X的化学式为 .