题目内容
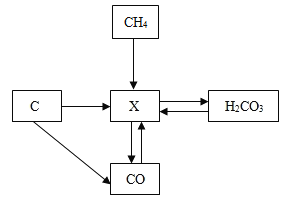
【题目】甲、乙、丙是初中化学常见三种物质,甲、乙、丙含有相同的一种元素,且丙是一种气体单质,甲和乙常温下是液体,它们相互转化关系如图所示。
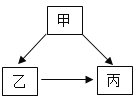
(1)则甲的化学式为___________。
(2)甲转化为丙的文字表达式为__________,其基本反应类型为_______。
【答案】H2O2 过氧化氢![]() 水 + 氧气 分解反应
水 + 氧气 分解反应
【解析】
甲、乙、丙含有相同的一种元素,且丙是一种气体单质,则丙可能是氧气,甲能转化生成乙和丙,乙能转化为丙,过氧化氢在二氧化锰催化作用下分解生成水和氧气,水通电时成氢气和氧气,则甲可能是过氧化氢,乙可能是水,代入框图,推断合理。
根据以上分析可知:
(1)甲是过氧化氢,其化学式为:H2O2;
(2)甲转化为丙的反应是过氧化氢在二氧化锰催化作用下分解生成水和氧气,其文字表达式为:过氧化氢![]() 水 + 氧气,该反应是由一种物质生成两种物质的反应,其基本反应类型为分解反应。
水 + 氧气,该反应是由一种物质生成两种物质的反应,其基本反应类型为分解反应。

 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】化学兴趣小组对“暖宝宝”的发热原理进行探究。
查阅资料:某品牌“暖宝宝”的主要成分为铁粉、水、食盐、活性炭、蛭石、吸水性树脂。食盐对铁粉生锈有催化作用;蛭石是一种优良的保温材料;吸水性树脂具有特强吸水、保水能力,且可反复释水、吸水。
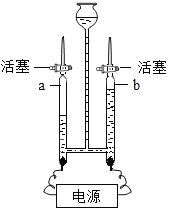
实验探究:小组同学利用图1所示的装置,完成下列表格中的3个实验。测得锥形瓶内温度随时间变化的图像如图2所示。
实验 | 放入锥形瓶中的物质 |
1 | 5 g铁粉、1 g氯化钠 |
2 | 5 g铁粉、1 g氯化钠、1.5 mL水 |
3 | 5 g暖宝宝袋内物质 |
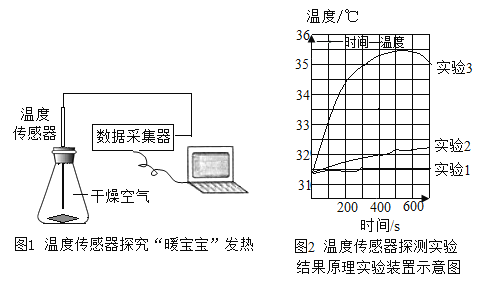
(1)实验1中温度几乎不变的原因是______。
(2)能证明实验2中物质发生反应的依据是_____。
(3)“暖宝宝”中活性炭的作用是_____。
(4)“暖宝宝”发热的原理是:①2Fe+O2+2H2O=2Fe(OH)2;②4Fe(OH)2+O2+2H2O=4Fe(OH)3;③2Fe(OH)3=Fe2O3+3H2O打开使用后的“暖宝宝”可观察到固体为红棕色,则该物质可能是___。
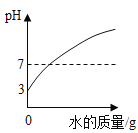
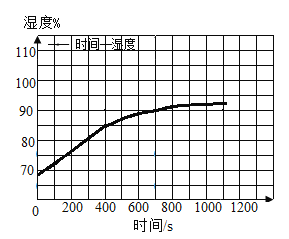
(5)将温度传感器改为湿度传感器,重复实验3,得到的数据如图所示。造成湿度逐渐增大的原因可能与“暖宝宝”中有关的成分是__。
(6)从能量转化角度,“暖宝宝”发热的实质是将____能转化为___能。
(7)“暖宝宝”贮存与使用时应注意的事项是____(写1种)。