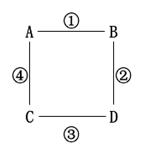
题目内容
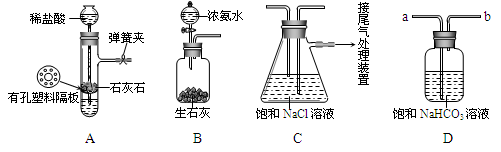
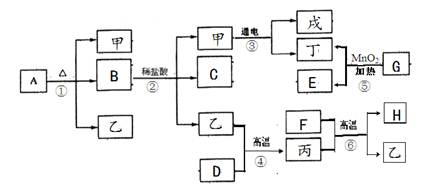
某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A﹣H编号后,做如下实验.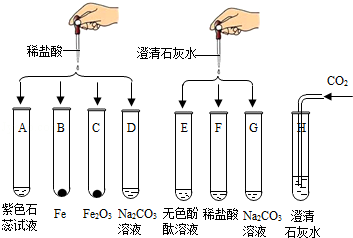
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 .
(2)实验后某试管中为红色溶液,当向其中加入过量的NaOH溶液后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是 .
(3)写出实验中无明显现象产生的试管中发生的化学方程式 .
(1)BD,GH;(2)紫色石蕊溶液;(3)2HCl+Ca(OH)2═CaCl2+2H2O
解析试题分析:(1)实验中观察到有气泡出现的试管是:BD,因为B中是铁和盐酸生成氯化亚铁和氢气,D中是碳酸钠和盐酸反应生成氯化钠和水和二氧化碳;有沉淀生成的试管是GH,因为G中碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,H中二氧化碳能使澄清的石灰水变浑浊;
(2)在A试管中盛有紫色石蕊试液,加入盐酸后,显酸性,酸能使紫色石蕊试液变红色,再向其中加入氢氧化钠溶液,当氢氧化钠把盐酸反应掉后,显碱性时,碱能使紫色石蕊试液变蓝色;
(3)实验中无明显现象产生的试管是F,发生的是盐酸与氢氧化钙反应生成氯化钙和水,反应的方程式为:Ca(OH)2+2HCl=CaCl2+2H2O
考点:探究酸碱的主要性质;书写化学方程式、文字表达式、电离方程式.
点评:本考点探究了酸和碱的化学性质,熟练掌握酸和碱的性质及两两反应的现象并正确书写化学方程式是解题的关键,难度不大.

 暑假作业安徽少年儿童出版社系列答案
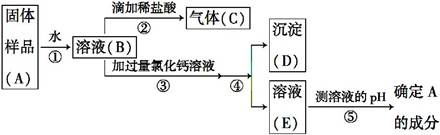
暑假作业安徽少年儿童出版社系列答案(7分)课外小组同学在实验室发现了一瓶标签残缺的无色液体(下图),想通过探究确定其成分,以便重新利用。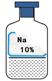
【初步分析】操作不规范可能造成标签破损,能造成标签破损的不当操作有 (写一点)。根据受损标签的情况判断,这瓶试剂不可能是 (填字母代号)。
A.酸 B.碱 C.盐
【查阅资料】初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。有关四种物质的信息如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 20oC溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 水溶液的pH | 7 | 14 | 11 | 9 |


(1)实验①观察到紫色石蕊试液变蓝,由此得出结论是 。
(2)实验②观察到有气泡产生,还有可能观察到的现象是 。
【得出结论】通过以上活动,小刚认为不能确定瓶中试剂的成分,小芳认为可以,小芳的理由是 。
【拓展应用】通过以上探究活动,小组同学联想到二氧化碳与氢氧化钠的反应,设计了如图丙所示实验,观察到的现象是 。
学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究.
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显 性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有 产生,说明小苏打能与酸反应.在医疗上可以用小苏打治疗 ;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她如图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成.当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl.小刚认为猜想 一定不正确,理由是 .小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为 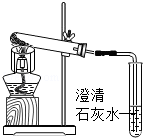
(4)小美和小刚继续探究固体成分,设计了如下实验:
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加 溶液 | 产生白色沉淀 | 试管内剩余的固体为Na2CO3 |
通过实验证明小苏打受热会分解,反应的化学方程式为: .通过本次探究学习,小美对小苏打的性质有了全面的认识,她给妈妈提出保存小苏打的建议有: (答出一点即可).