题目内容
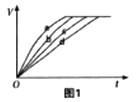
【题目】等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是

A. 相对原子质量较大的是N
B. 生成H2的质量M<N
C. M、N两种金属中较活泼的是N
D. 产生H2的反应速率是N>M
【答案】A
【解析】A、设M、N的质量都是z,相对原子质量为x、y,生成氢气的质量为m、n,
M+2HCl═MCl2+H2↑,N+2HCl═NCl2+H2↑,
x 2 y 2
z m z n
x=![]() ,y=
,y=![]() ,
,
因为m>n,所以x<y,即N的相对原子质量大于M的相对原子质量,故A正确;
B、由图中信息可知,M与稀盐酸反应生成氢气的质量大,故B错误;
C、由图中信息可知,M与稀盐酸反应的速率快,说明M比N活泼,故C错误;
D、由图中信息可知,M与稀盐酸反应生成氢气的速率快于N和稀盐酸反应生成氢气的速率,故D错误.
故选:A.

【题目】等质量的铁粉与过量的盐酸在不同的实验条件下进行反应,测定在相同时间t产生气体体积V的数据,根据数据绘制得到图1。
组别 | 盐酸的溶质质量分数 | 温度(℃) |
① | 7 | 30 |
② | 10 | 50 |
③ | 7 | 20 |
④ | 10 | 30 |
(1)请写出铁粉稀盐酸反应的化学方程式。
(2)由实验(填组别)可知,温度对于金属与酸反应速率的影响是。
(3)图1中表示第3组实验的曲线是。
(4)[进一步探究]图甲、图乙为利用数字化仪器测得的室温下足量的三种金属片分别与200ml100℅的稀盐酸反应产生氢气的量。(产生氢气的量由气体压强表示,在等温条件下,产生氢气体积与装置内压强成正比)。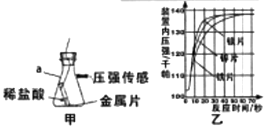
①实验中你认为,还要控制的变量是。
②由图乙,你得出的反应物的量与生成的气体体积的关系是。
(5)[拓展提高]下图为测得的室温下足量的镁片与20ml110℅的稀盐酸反应产生氢气的量与时间关系曲线,发现实验测得的实际值比通过计算得到的理论值偏大,请分析可能的原因(至少答两点)。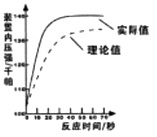
①。
②。