题目内容
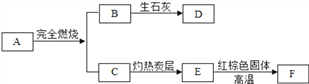
【题目】粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2、MgCl2)。现以粗盐为原料制取精盐,生产过程如图所示
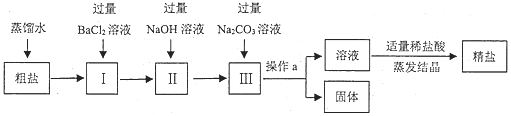
(1)写出I中发生反应的化学方程式__________;
(2)操作a的名称是_____,该操作需要用到的玻璃仪器主要有:烧杯、___、玻璃棒;
(3)加入适量稀盐酸的作用是除去溶液中的_______________(填化学式);
(4)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是_______________。
【答案】 BaCl2+ Na2SO4== BaSO4↓+ 2NaCl 过滤 漏斗 NaOH、Na2CO3 防止受热不均,使液滴飞溅
【解析】(1)I中发生反应是氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,化学方程式BaCl2+ Na2SO4== BaSO4↓+ 2NaCl;(2)操作a的名称是过滤,该操作目的是将沉淀和液体分离,需要用到的玻璃仪器主要有:烧杯、漏斗、玻璃棒;(3)加入适量稀盐酸的作用是除去溶液中的因过量引入的氢氧化钠(NaOH)和碳酸钠(Na2CO3);(4)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是防止液体受热不均,使液滴飞溅。

 全能练考卷系列答案
全能练考卷系列答案【题目】合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特征的物质。一般来说,合金的熔点低于任何一种组分金属的熔点。 下表是一些金属的熔点数据。
金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
熔点/℃ | 1 083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
(1)铅锡合金中某种金属的质量分数与合金的熔点有如图所示的关系,其中横坐标表示的是________的质量分数;当合金熔点最低时,合金中铅与锡的质量比为________。
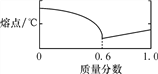
(2)保险丝由铋、铅、锡、镉等金属组成,其熔点约为________。
A.20~40 ℃ B.60~80 ℃ C.230~250 ℃ D.300~320 ℃