题目内容
【题目】有A、B、C、D、E五种物质,暗紫色的固体A受热会产生一种是带火星木条复燃的气体B,黑色固体C在B中燃烧,发出白光,生成使澄清石灰水变浑浊的气体,银白色金属D在B中剧烈燃烧,火星四射,生成黑色固体E。
(1)写出各物质的化学式(符号):A________,B________,C________,D________,
(2)写出D在B中燃烧的文字或符号表达式___________________。
【答案】KMnO4 O2 C Fe 铁+氧气![]() 四氧化三铁或Fe+O2
四氧化三铁或Fe+O2![]() Fe3O4
Fe3O4
【解析】
B能使带火星的木条复燃,得知B是氧气;黑色固体C在氧气中燃烧,发出白光,生成使澄清石灰水变浑浊的气体,则C为木炭,银白色金属D在氧气中剧烈燃烧,火星四射,生成黑色固体E.则D为铁丝,E为四氧化三铁;暗紫色的固体A受热会产生氧气,则A为高锰酸钾.
(1)由上述分析可知 A为KMnO4,B为O2,C为C,D为Fe;
(2)铁丝在氧气中燃烧生成四氧化三铁,文字表达式或符号表达式为铁+氧气![]() 四氧化三铁或Fe+O2
四氧化三铁或Fe+O2![]() Fe3O4。
Fe3O4。

【题目】某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表。
样品 | 第1份 | 第2份 | 第3份 | 第4份 |
取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
试计算:
⑴根据测得的数据分析,第1份样品中 (填物质)完全反应了。
⑵列式计算黄铜屑样品中的锌的质量分数。
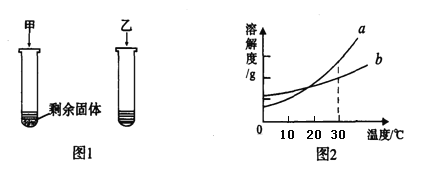
⑶请在图中画出在50.0g样品中加稀硫酸的质量与产生气体质量变化关系的示意图。
【题目】某矿石主要成分是MgO,含少量的Fe2O3、CuO和SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图:
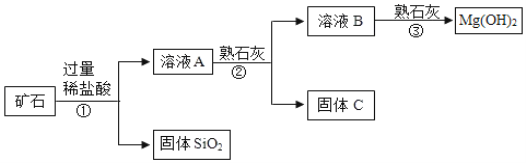
回答下列问题:
(1)步骤①中发生反应的方程式_____(任写一个)。
(2)溶液A中所含的阳离子有_____(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的pH应为:_____≤PH<_____,固体C中所含成分的化学式为_____、_____。
(4)步骤③制得Mg(OH)2的化学方程式为_____。