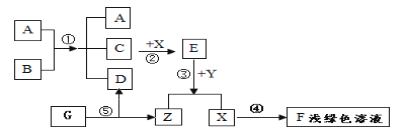题目内容
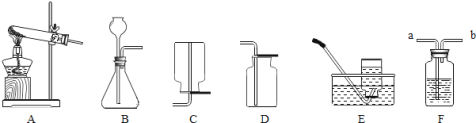
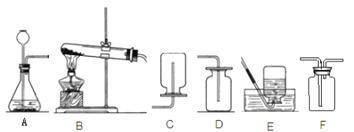
【题目】(7分)如图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:
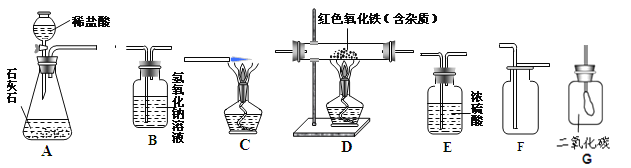
(1)欲在实验室中制备并收集干燥的二氧化碳气体。
①所选仪器的连接顺序为_________________(填写仪器序号字母)。
②仪器A中,发生反应的化学方程式为____________________ __________。
③若向G装置中倒入适量澄清石灰水,迅速用预先绑有小气球的橡皮塞塞紧,振荡,观察到的气球出现的现象是 。
(2)欲用混有少量二氧化碳的一氧化碳气体测定10g某不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:混合气体→D→B→C。
①进行实验时,要先向D装置的玻璃管中通一会儿CO,然后加热,理由是____________________。
②通过测量反应前、后D装置处大玻璃管的质量变化,来计算氧化铁样品的纯度。若反应前后D装置的质量减少2.4g,则该氧化铁样品的纯度为 。
③若通过测量反应前、后B装置的质量变化,来计算氧化铁样品的纯度,则计算出样品纯度的结果将__________ (填“偏大”、“偏小”、“不影响”其中之一)。
【答案】(1)①A→E→F ②CaCO3+2HCl CaCl2+H2O+CO2↑. ③气球鼓起 (2)① 排净玻璃管中的空气,防止加热时发生爆炸 ② 80% (3)偏大.
【解析】
试题分析:(1)①实验室用石灰石和稀盐酸制取二氧化碳,选用发生装置A,二氧化碳能溶于水,要用向上排空气法收集,连接顺序为:A→E→F ②碳酸钙和盐酸反应生成二氧化碳、水、氯化钙,CaCO3+2HCl CaCl2+H2O+CO2↑; ③二氧化碳和石灰水反应,瓶内气体减少,压强变小,小于外界大气压,故气球鼓起 (2)① 先向D装置的玻璃管中通一会儿CO,排净玻璃管中的空气,防止加热时发生爆炸 ②反应前后D装置的质量减少2.4g是氧化铁中氧元素的质量,所以氧化铁的质量=2.4g÷30%=8g,样品中氧化铁的含量=8g÷10g×100%= 80% (3)若通过测量反应前、后B装置的质量变化,来计算氧化铁样品的纯度,由于B不仅吸收了生成的二氧化碳,还能吸收空气中的二氧化碳,导致计算结果偏大

 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案