题目内容
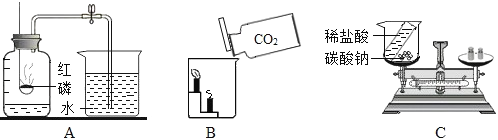
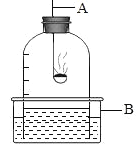
【题目】如图是某学校的老师做的测定空气中氧气含量的演示实验,仔细观察该实验装置,请你回答下列问题:
①写出仪器的名称:A_____,B_____。
②盛放在仪器A中的物质是_____,该物质燃烧的现象是_____。
③在实验中,钟罩内的水面所发生的变化是_____。
④在实验中,若仪器A中的物质太少,测得的氧气体积百分比将会_____;若钟罩的气密性不好,测得的氧气体积百分比将会_____。(填“偏大”或“偏小”或“不变”)
【答案】燃烧匙;水槽;红磷;发黄光、冒白烟;实验开始时,钟罩内的液面下降,实验结束后,钟罩内液面上升,上升的水的体积约占钟罩内空气体积的五分之一;偏小;偏小。
【解析】
①A是燃烧匙,B是水槽;②在实验室中,常用红磷测定空气中氧气的含量,红磷燃烧发出黄光、冒出白烟;③红磷燃烧发出热量,导致钟罩内的气体体积膨胀,压强增大,钟罩内的液面下降;红磷熄灭后,温度冷却至室温,由于钟罩内的氧气被完全耗尽,压强减小,钟罩内的液面上升,由于氧气约占空气体积的五分之一,所以观察到实验开始时,钟罩内的液面下降,实验结束后,钟罩内液面上升,上升的水的体积约占钟罩内空气体积的五分之一;④用红磷测定空气中氧气的体积分数时,所用红磷的量不足,空气中氧气不能完全耗尽,使所测得氧气的体积分数偏小。要使本实验成功,必须注意以下几点:装置的气密性好;红磷足量;必须冷却到室温再读数,要不然都会使测定的结果偏低。

【题目】为测定某黄铜(铜锌合金)样品中铜的含量,某化学活动小组分三次进行实验,实验数据如表,请回答下列问题:
所取药品 | 第一次 | 第二次 | 第三次 |
黄铜样品质量(g) | 12 | 10 | 10 |
稀盐酸质量(g) | 100 | 100 | 150 |
生成气体质量(g) | 0.2 | 0.2 | 0.2 |
(1)第____次实验中,药品成分恰好完全反应。
(2)黄铜样品中铜的质量分数是多少?恰好完全反应时所得溶液的溶质质量分数是多少________?(精确到0.1%)
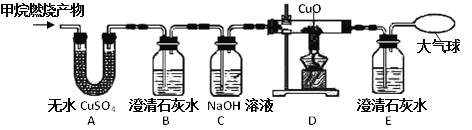
【题目】某化学兴趣小组用一定浓度的稀盐酸和含杂质5%(杂质不与盐酸反应)的石灰石制备CO2,他们选择的制取和收集装置如图所示。请按要求回答问题和探究:

(1)装置A中仪器a的名称是___,若要制取并收集干燥的CO2,导管的连接顺序是___。
(2)若消耗的石灰石为100g,理论上可得到CO2___g(精确到0.1),但实际收集到的CO2质量与理论值不符,原因可能是___(填一种)。
(3)探究装置A中残留液的溶质成分。
(提出问题)残留液中含有哪些溶质?
(查阅资料)CaCl2溶液呈中性。
(思考判断)残留液中一定含有的溶质是___(填物质名称),可能含有的溶质是HCl。
(实验验证)同学们通过多种实验方法,均验证了残留液中的溶质有HCl,请完成下表。
实验操作 | 现象(数据或化学方程式) | 结论 | |
方法一 | 用酸碱指示剂测定溶液的酸碱性,所选择的指示剂为___。 | 现象:___ | 残留液中的溶质有HCl |
方法二 | 用pH试纸测定溶液的pH。 | pH___ 7 (填“>”“=”或“<”) | |
方法三 | 用化学药品检测,且发生了复分解反应,可能选用的药品为___(填一种物质的化学式)。 | 现象:___ 化学方程式:___ |