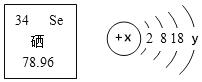题目内容
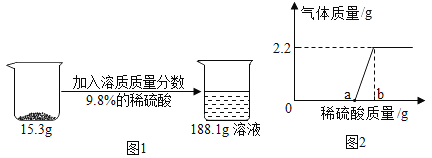
【题目】我市某校化学兴趣小组利用图装置进行“硫燃烧现象及酸雨危害模拟”实验,
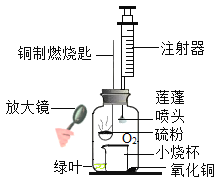
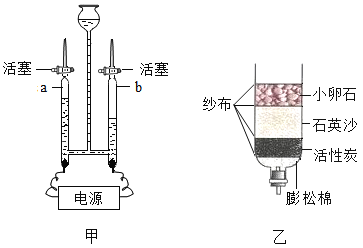
(1)按图装置连接仪器,装好药品,塞紧胶塞;
(2)用放大镜聚强光引燃硫粉,可观察到硫粉燃烧时发出明亮的_______色火焰
(3)冷却后,用注射器向广口瓶中喷水,可观察到:
①绿叶变黄 ②小烧杯里收集到一定量的液体; ③氧化铜粉末逐渐消失,溶液变成蓝色.
(4)取出小烧杯里收集到的液体进行检验,结果该溶液为酸性(样品)
(提出问题)小烧杯里刚收集到的样品中溶质是什么?
(查阅资料)①SO2易溶于水,化学性质与二氧化碳有相似之处;②H2SO3易被氧化物为H2SO4;③BaSO3不溶于水,能与盐酸反应;BaSO4既不溶于水,也不溶于盐酸.
(作出猜想)
猜想Ⅰ:样品中溶质含有H2SO3;猜想Ⅱ:样品中溶质含有H2SO4;猜想Ⅲ:样品中溶质含有_______________________(填化学式)
(实验探究)
实验操作 | 实验现象 | 实验结论 |
向刚收集到的样品中滴加过量的Ba(OH)2溶液,过滤 | 有白色沉淀生成 | 猜想 _________正确 |
向白色沉淀中加入足量的 _________ | 沉淀不溶解 |
(交流讨论)
(1)向刚收集到的样品中滴加过量的Ba(OH)2溶液的目的是_____________________
(2)酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于___________
(拓展延伸)
SO2气体可用氢氧化钠溶液吸收,反应原理是______________(用化学方程式表示)
【答案】蓝紫 H2SO3和H2SO4 稀盐酸 Ⅱ 让样品中的溶质完全反应生成沉淀 置换反应 2NaOH+SO2=Na2SO3+H2O
【解析】
(2)硫在氧气中燃烧时,发出明亮的蓝紫色火焰,并放出热量;故填:蓝紫。
[作出猜想]酸雨中的溶质可能是H2SO4;也可能是H2SO3;还可能既有H2SO3又有H2SO4;故填:H2SO3和H2SO4。
[实验探究]H2SO3和H2SO4都能与Ba(OH)2反应生成白色沉淀,但BaSO3不溶于水,能与盐酸反应;BaSO4既不溶于水,也不溶于盐酸;所以可向样品中加入Ba(OH)2生成白色沉淀,再用盐酸验证白色沉淀是BaSO3还是BaSO4,或者两种都有,从而验证样品中溶质的成分。
向沉淀中加入足量稀盐酸,沉淀不溶解说明沉淀中只有硫酸钡,故填:Ⅱ。
[交流讨论]
(1)向刚收集到的样品中滴加过量的Ba(OH)3溶液的目的是让样品中的溶质完全反应生成沉淀;
故填:让样品中的溶质完全反应生成沉淀。
(2)酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于置换反应;故填:置换反应。
[拓展延伸]
二氧化硫与氢氧化钠反应生成亚硫酸钠和水,反应的化学方程式为:2NaOH+SO2=Na2SO3+H2O;故填:2NaOH+SO2=Na2SO3+H2O。

【题目】水是生命之源,人类的日常生活与工农业生产都离不开水。
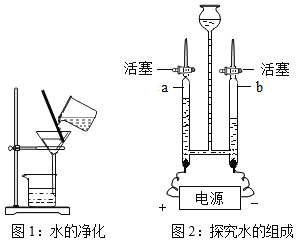
(1)化学课上同学们分组研究水的净化及组成。其中一组同学用自制简易净水器净化池塘水(图①所示)。现有:①净化后的池塘水、②矿泉水、③蒸馏水、④自来水四种水,其中属于纯净物的是__ __(填标号)。检验自来水是硬水还是软水,可选用的物质是 。生活中既能降低水的硬度,又能杀菌消毒的方法是 。
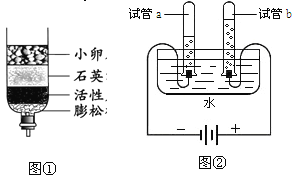
(2)实验中通电一段时间后(图②所示),试管b中气体的气体是 (填写化学式),可用 方法检验,该实验说明水是由 组成的。
(3)小华同学用图②所示的装置进行电解水实验,有以下描述:①向水中加入少量硫酸,能使水电解产生气体的速度加快 ②试管a、b两试管内收集到的气体的体积比约为2:1 ③a试管内产生的气体能燃烧 ④a、b两试管内产生的气体的质量比约为1:8。以上描述中正确的是 。
A.③ | B.①②③④ | C.①② | D.①②③ |
(4)小明同学收集到一杯有臭味的浑浊污水,先用滤纸进行过滤,过滤时所用的玻璃仪器有烧杯、玻璃棒和 ,过滤后发现水虽然变清,但是依旧有臭味,能够除去臭味的方法是 。
(5)从微观角度分析,图①和图②发生的变化中最本质的区别是 。
(6)重水可用作核反应堆中的减速剂,构成重水的氢原子与普通水中的氢原子不同。一个重水分子是由两个重氢原子和一个氧原子构成的,重氢原子的核电荷数是1,核内中子数是1,那么一个重水分子比一个普通水分子多 个中子。