题目内容
【题目】如图 1 是实验室常用的制取气体的装置,请回答下列问题:
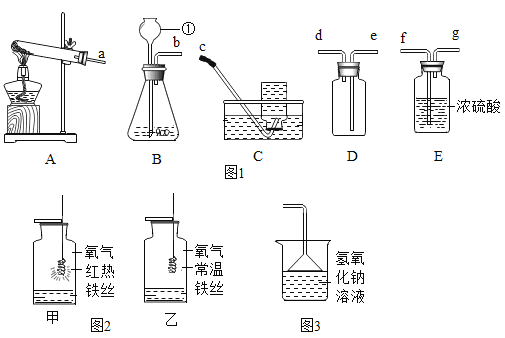
(1)写出图 1 中仪器①的名称_____。
(2)实验室制取二氧化碳气体时,应选择的发生装置是_____ (填字母序号),反应的化学方程式为_____。
(3)实验室用 A 装置制取氧气时,试管口略向下倾斜的原因是_____; 可以用 C 装置收集氧气的原因是_____。
(4)图 2 装置是铁丝在氧气中燃烧的实验,甲中的实验现象是_____。 通过该实验说明可燃物燃烧需要满足的一个条件是_____。
(5)氯气(Cl2)是一种黄绿色、有刺激性气味的有毒气体,密度比空气大,极易溶于水。
①实验室可用高锰酸钾和浓盐酸制取氯气,若选用图 1 中的装置制取并收集一瓶干燥的氯气,装置导管口的连接顺序应为_____(填字母序号)。
②氯气排放到空气中会污染环境,实验室常用图3装置吸收多余的氯气,由此说明氯气具有的化学性质是_____。
【答案】长颈漏斗 B CaCO3+2HCl=CaCl2+H2O+CO2![]() 防止冷凝水倒流,炸裂试管 氧气不易溶于水且不与水反应 剧烈燃烧,放出热量、火星四射,产生黑色固体 温度达到着火点以上 bfged 能与氢氧化钠溶液反应
防止冷凝水倒流,炸裂试管 氧气不易溶于水且不与水反应 剧烈燃烧,放出热量、火星四射,产生黑色固体 温度达到着火点以上 bfged 能与氢氧化钠溶液反应
【解析】
(1)由常见的仪器可知,仪器①的名称是长颈漏斗;故填:长颈漏斗。
(2)实验室制取二氧化碳气体采用的是大理石和稀盐酸反应,该反应在常温下进行,因此选用的发生装置是B;大理石和稀盐酸反应生成氯化钙、水和二氧化碳气体,其化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2![]() 。故填:B;CaCO3+2HCl=CaCl2+H2O+CO2
。故填:B;CaCO3+2HCl=CaCl2+H2O+CO2![]() 。
。
(3)加热固体时,会产生水蒸气,水蒸气冷凝回流后遇到热的试管,会使试管炸裂;故加热时试管口应略向下倾斜的原因是:防止冷凝水倒流,炸裂试管;C装置收集氧气的方法是排水法,所以能采用C装置收集氧气的原因是:氧气不易溶于水且不与水反应;
(4)甲中红热的铁丝在氧气中剧烈燃烧,放出热量,火星四射,产生黑色固体;甲实验中红热的铁丝,铁丝燃烧,乙实验中常温的铁丝,铁丝不燃烧,通过两实验的比较可以得出可燃物燃烧需要温度达到着火点以上;故填:剧烈燃烧,放出热量,火星四射,产生黑色固体;温度达到着火点以上。
(5)①实验室用高锰酸钾和浓盐酸在常温的条件下制取氯气,可以选择B为发生装置,可以用浓硫酸来干燥气体,干燥装置选用E,气体应从长管通入;由于氯气的密度比空气大,极易溶于水,因此可以采用向上排空气法来收集,收集装置选用D,气体应从长管通入;因此若选用图1中的装置制取并收集一瓶干燥的氯气,装置导管口的连接顺序应为bfged。故填:bfged。
②从图3装置中采用氢氧化钠溶液来作吸收液,可以看出氯气可以与氢氧化钠溶液发生化学反应,从而起到吸收的作用;故说明氯气具有的化学性质是能与氢氧化钠发生反应。故填:能与氢氧化钠溶液反应。

【题目】某学习小组拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。查阅资料可知 Mg、Mg3N2能发生如下反应:
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]()
实验中所用的装置和药品如图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。回答下列问题:
(1)连接并检查实验装置的气密性,实验开始时,将空气通入实验装置,则气流流经装置的顺序是_____(填装置序号)。D装置中发生反应的化学方程式为_____。
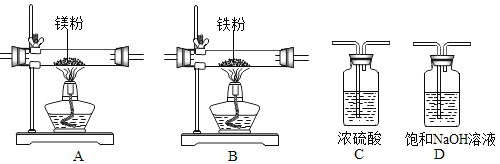
(2)通气后,应先点燃_____(填“A”或“B”)装置的酒精灯,如果同时点燃A、B装置的酒精灯,对实验结果有何影响?_____。
(3)设计一个实验,验证产物是氮化镁:
实验操作和实验现象 | 实验结论 |
_____ | 产物是氮化镁 |
(4)思维拓展:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N2的质量,请给出合理的解释_____。