题目内容
【题目】根据图中所示装置回答下列问题:
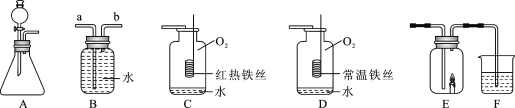
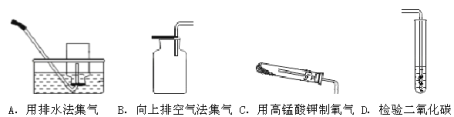
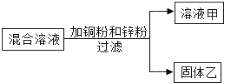
(1)若用装置B排水法收集氧气,气体应从_____(填“a”或“b”)导管通入瓶内;瓶底留有少量水进行装置C中的实验,水的作用是______________________________。
(2)对比装置D和C,可以得出关于可燃物燃烧的条件是_________________________。
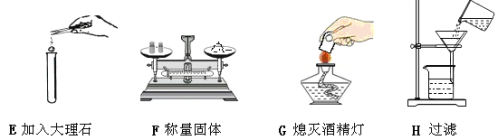
(3)两名同学分别连接A、E、F进行实验,A中所加药品不同,F中所加药品相同。
①若实验时E中蜡烛熄灭,F中溶液变浑浊,则A中反应的化学方程式为________________;E中蜡烛熄灭,说明A中产生的气体所具有的性质为___________、____________。
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,则A中反应的化学方程式为_____________F中反应的化学方程式为_______________________________。
【答案】b 防止高温下的生成物炸裂瓶底 温度达到可燃物的着火点 CaCO3+2HCl=CaCl2+H2O+CO2↑ 不燃烧 不支持燃烧 2H2O2![]() 2H2O+O2↑ CO2+Ca(OH)2=CaCO3↓+H2O
2H2O+O2↑ CO2+Ca(OH)2=CaCO3↓+H2O
【解析】
铁在氧气中点燃生成四氧化三铁,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,过氧化氢在二氧化锰催化作用下生成水和氧气,二氧化碳和氢氧化钙反应生成碳酸钙和水。
(1)氧气的密度比水小,氧气从短管进,水从长管排出,故若用装置B排水法收集氧气,气体应从b导管通入瓶内;铁在氧气中点燃生成四氧化三铁,放出大量热,故瓶底留有少量水进行装置C中的实验,水的作用是防止高温下的生成物炸裂瓶底。
(2)燃烧的条件是物质是可燃物、温度达到可燃物着火点、有氧气参与,装置C温度较高,其他和装置D相同,故对比装置D和C,可以得出关于可燃物燃烧的条件是温度达到可燃物的着火点。
(3)①若实验时E中蜡烛熄灭,F中溶液变浑浊,说明生成二氧化碳,二氧化碳不燃烧、不支持燃烧,二氧化碳能使澄清石灰水变浑浊,则A中反应是碳酸钙和稀盐酸生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;E中蜡烛熄灭,说明A中产生的气体所具有的性质为不燃烧、不支持燃烧。
②若实验时E中蜡烛燃烧更旺,F中溶液变浑浊,说明反应装置生成氧气,蜡烛燃烧生成二氧化碳,则A中反应是过氧化氢在二氧化锰催化作用下生成水和氧气,反应的化学方程式为2H2O2![]() 2H2O+O2↑,F中反应是二氧化碳和氢氧化钙生成碳酸钙和水,反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O。
2H2O+O2↑,F中反应是二氧化碳和氢氧化钙生成碳酸钙和水,反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O。

【题目】下列实验中,现象与结论对应关系正确的是
A | B | C | D | |
图示 |
|
|
|
|
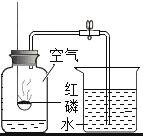
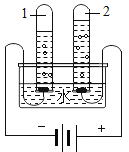
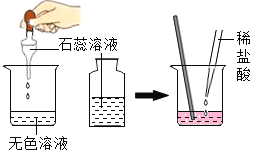
现象 | 铜片上白磷燃烧红磷不燃烧,水中白磷不燃烧 | 冷却后,打开弹簧夹,水被吸入瓶内,瓶内水面上升约 1/5 | 试管 1 中的气体燃烧,产生淡蓝色火焰,试管 2 中的气体能使带火星的木条复燃 | 滴有石蕊的溶液呈蓝色,加入稀盐酸后蓝色变为红色 |
结论 | 水中白磷不燃烧,因为没有达到着火点 | 氧气约占空气质量的 1/5 | 水是由氧气和氢气组成的 | 反应后的溶液中一定不含碱性物质 |
A.AB.BC.CD.D
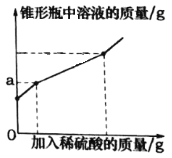
【题目】为测定久置于空气中的氢氧化钠样品的变质程度,某化学活动小组称取该固体样品6.5g放入锥形瓶中,加水溶解,配成50g溶液,再向锥形瓶中滴加稀硫酸,反应过程中产生气体质量的部分实验数据和锥形瓶中溶液质量变化的图象如表所示:
加入稀硫酸的质量/g | 40 | 65 | 75 |
产生气体的质量/g | 1.1 | 2.2 | 2.2 |
(1)6.5g样品与稀硫酸完全反应产生气体的质量是________g。
(2)6.5g样品中碳酸钠的质量分数是________。(结果精确至0.1%)
(3)以上三次的实验数据中,只有一次加入的稀硫酸与锥形瓶中溶液的溶质恰好完全反应。
①如图图象中a的数值是________。
②求该实验中所用稀硫酸的溶质质量分数____。(写出计算过程)