题目内容
【题目】(6分)如图是某胃药标签的部分内容。小明同学测定该药品中NaHCO3含量的过程如下:取10粒该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5克。称得反应后烧杯内物质的总质量为64.3克。

请计算:(1)反应完成后生成气体的质量为 g。
(2)反应后烧杯中溶液的质量和胃药中NaHCO3的质量分数。
【答案】(1)2.2; (2)84%
【解析】
试题分析:(1)每粒0.5g,10粒该药剂的质量为0.5g×10=5g.
由质量守恒定律,生成二氧化碳气体的质量为5g+50g+11.5g﹣64.3g=2.2g.
(2)设参加反应的碳酸氢钠的质量为x,
NaHCO3+HCl=NaCl+H2O+CO2↑
84 44
x 2.2g
x=4.2g
反应后烧杯中溶液的质量为4.2g+50g+11.5g﹣2.2g=63.5g.
胃药中NaHCO3的质量分数为4.2g/5.5g×100%=84%.
答:(1)2.2g;(2)反应后烧杯中溶液的质量为63.5g;胃药中NaHCO3的质量分数为84%.

 阅读快车系列答案
阅读快车系列答案【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
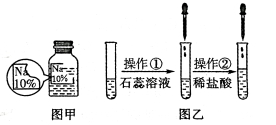
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。