题目内容
【题目】某实验小组对实验室制取氢气的反应原理进行探究。
【知识回顾】能产生氢气的化学反应有: ①水电解 ②活泼金属与酸反应
【讨论交流】反应①的化学方程式 ;同学们讨论后认为该反应不适用于实验室制取氢气。
【实验探究】为了探究哪种物质更适合用于实验室制取氢气,大家设计了如下实验:
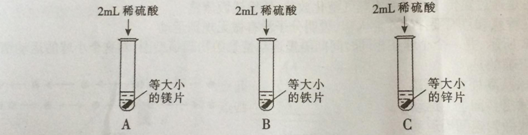
【分析与结论】填写实验报告。
实验 | 实验现象 | 实验结论 |
A | 剧烈反应,迅速产生大量气泡,试管外壁 | 反应速率过快,气体不便收集,不能用于实验室制取氢气 |
B | 缓慢产生少量气泡 | 反应速率过慢,不能用于实验室制取氢气 |
C | 较快产生大量气泡,试管外壁发热 |
通过实验得出,适合实验室制取氢气的化学反应方程式为 ;
【知识拓展】(1)确定实验室制取气体的反应原理时,要考虑诸多因素,如反应的快慢、收集的难易、 等。
(2)用稀盐酸制取氢气时,制得的气体中可能会增加的杂质为 。
【答案】【讨论交流】2H2O![]() 2H2↑+ O2↑(2分) 【分析与结论】A的实验现象:发烫;C的实验结论:反应速率适中,适用于实验室制取氢气;Zn + H2SO4 == ZnSO4 + H2↑【知识拓展】(1)反应条件(或成本、气体纯度等)(2分)(2)氯化氢(或HCl)
2H2↑+ O2↑(2分) 【分析与结论】A的实验现象:发烫;C的实验结论:反应速率适中,适用于实验室制取氢气;Zn + H2SO4 == ZnSO4 + H2↑【知识拓展】(1)反应条件(或成本、气体纯度等)(2分)(2)氯化氢(或HCl)
【解析】
试题分析: 根据电解水的实验可以得到【讨论交流】反应①的化学方程式为2H2O![]() 2H2↑+ O2↑;【分析与结论】根据金属与酸反应的现象和金属活动性顺序可知,实验A中实验现象为剧烈反应,迅速产生大量气泡,试管外壁发烫;实验C的实验现象为较快产生大量气泡,试管外壁发热,可得出结论为反应速率适中,适用于实验室制取氢气;通过实验得出,适合实验室制取氢气的化学反应方程式为Zn + H2SO4 == ZnSO4 + H2↑;【知识拓展】(1)确定实验室制取气体的反应原理时,要考虑诸多因素,如反应的快慢、收集的难易、反应条件(或成本、气体纯度等)等。(2)用稀盐酸制取氢气时,制得的气体中可能会增加的杂质为挥发出的氯化氢气体。
2H2↑+ O2↑;【分析与结论】根据金属与酸反应的现象和金属活动性顺序可知,实验A中实验现象为剧烈反应,迅速产生大量气泡,试管外壁发烫;实验C的实验现象为较快产生大量气泡,试管外壁发热,可得出结论为反应速率适中,适用于实验室制取氢气;通过实验得出,适合实验室制取氢气的化学反应方程式为Zn + H2SO4 == ZnSO4 + H2↑;【知识拓展】(1)确定实验室制取气体的反应原理时,要考虑诸多因素,如反应的快慢、收集的难易、反应条件(或成本、气体纯度等)等。(2)用稀盐酸制取氢气时,制得的气体中可能会增加的杂质为挥发出的氯化氢气体。

【题目】对下列各主题知识的整理完全正确的是( )
A | 环境保护 | B | 生活常识 |
废旧电池——随意丢弃 工业污水——处理后排放 | 防煤气中毒——室内放一盆水 人体缺铁——引起缺铁性贫血 | ||
C | 化学反应类型 | D | 性质与用途 |
盐酸和石灰水混合——中和反应 一氧化碳还原氧化铁——置换反应 | 甲烷有可燃性——用作燃料 活性炭有吸附性——用于净化水 |