题目内容
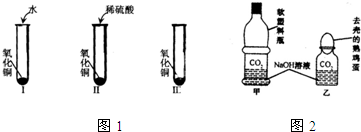
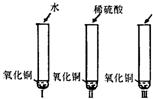 28、氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.
28、氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.【提出假设】你提出的假设是
稀H2SO4中的H+溶解CuO
.【设计实验】通过实验Ⅰ可证明
水不能溶解CuO
.要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和实验Ⅲ,在实验皿中应加入
稀盐酸或Na2SO4或硫酸钾或硫酸铜
【实验结果】探究结果为
稀H2SO4中的H+溶解CuO,H2O和SO42-不能溶解CuO
.请写出氧化铜与稀硫酸反应的化学方程式:
CuO+H2SO4═CuSO4+H2O
.分析:根据所学知识,学生知道稀硫酸中存在H+、SO42-、H2O三种粒子,提出假设并不困难,一般都知道应是三种粒子中的某一种使CuO溶解.关键是通过三组不同实验,根据不同的现象进行分析、对比得出是H+使CuO溶解的结论.题目中的Ⅰ实验证明了H2O不能使CuO溶解的结论,实验Ⅱ中既有H+,又有SO42-和H2O,其中水分子已经证明了不能使CuO溶解,因此实验Ⅲ就应该考虑单独含有H+或SO42-的物质和CuO反应,观察CuO是否溶解,所以实验Ⅲ中应加入的物质可以是稀盐酸或硫酸钠溶液,还能溶解CuO的另一种常见物质是硝酸或盐酸.
解答:解:由实验可知,①水不能溶解氧化铜;②氧化铜也不能溶解于硫酸钠(带有硫酸根的盐)溶液;③氧化铜能溶解于酸溶液.④写出氧化铜与稀硫酸反应的化学方程式,知道反应物,书写生成物,从而书写化学方程式.
故答为:【提出假设】稀H2SO4中的H+溶解CuO;
【设计实验】水不能溶解CuO;稀盐酸或Na2SO4或硫酸钾或硫酸铜;
【实验结果】稀H2SO4中的H+溶解CuO,H2O和SO42-不能溶解CuO;CuO+H2SO4═CuSO4+H2O
故答为:【提出假设】稀H2SO4中的H+溶解CuO;
【设计实验】水不能溶解CuO;稀盐酸或Na2SO4或硫酸钾或硫酸铜;
【实验结果】稀H2SO4中的H+溶解CuO,H2O和SO42-不能溶解CuO;CuO+H2SO4═CuSO4+H2O
点评:本题考查了如何探究物质的性质和变化规律,掌握猜想和实验验证的方法.

练习册系列答案
相关题目
 21、氧化铜是一种黑色固体,可溶于稀硫酸:某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过下图I、II、III三个实验完成这次探究活动.
21、氧化铜是一种黑色固体,可溶于稀硫酸:某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过下图I、II、III三个实验完成这次探究活动.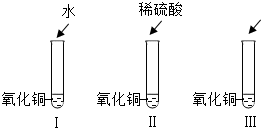 氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.