题目内容
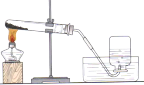
【题目】化学是一门以实验为基础的科学,化学所取得的丰硕成果,与实验的重要作用分不开。请根据下图回答问题:
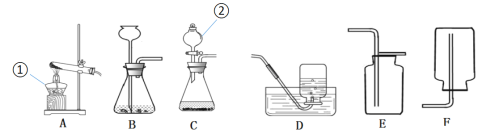
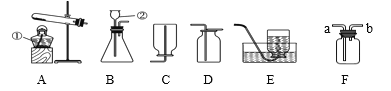
(1)写出图中数字②所代表的仪器名称:__________,
(2)若要在实验室用高锰酸钾制取并收集一瓶氧气,你应选择图中的_______(填字母序号)作为发生装置,其相应的文字表达式:________,如果要想收集到一瓶较干燥的氧气来做蜡烛在氧气中燃烧的实验,收集装置应选_____(填字母序号)。验证氧气的方法是__________。
(3)在化学分组实验课上,老师要求用过氧化氢溶液和二氧化锰来制取氧气,在选择发生装置时,小桐和小晨发生了争论。最后经讨论,他们选择了C装置,你认为他们选择C装置的理由是__________,该反应的化学式表达式为_____________。
(4)小桐选B装置用稀盐酸和石灰石制取二氧化碳,收集装置应选择______(填字母序号),检验二氧化碳是否收集满的方法是_____________。
(5)乙炔是一种无色、无味、密度比空气略小,不溶于水的气体。工业上常用它燃烧产生的高温来切割和焊接金属,实验室用电石(固体)与水在常温下反应(反应很剧烈)制取乙炔。你认为制取乙炔应选择的发生装置是_______(填字母序号),小明想收集到较纯净的乙炔气体,他应该选的收集装置是_______。
(6)下图所示装置是一个多用途的装置(又称万能瓶),当用于收集气体时既可以为排水法、又可以为向下排空气法和向上排空气法。现在小娟同学想用排空气法收集一瓶乙炔气体,在该装置不改变放置方式的情况下,她应将乙炔从______(选填“a”或“b”)端通入。

【答案】分液漏斗 A 高锰酸钾![]() 锰酸甲+二氧化锰+氧气 E 将带火星的木条伸入集气瓶内,木条复燃,证明是氧气 可以控制反应速率(合理均给分) H2O2
锰酸甲+二氧化锰+氧气 E 将带火星的木条伸入集气瓶内,木条复燃,证明是氧气 可以控制反应速率(合理均给分) H2O2 ![]() H2O + O2 E 把燃着的木条放在集气瓶口,木条熄灭,说明已收集满 C D b
H2O + O2 E 把燃着的木条放在集气瓶口,木条熄灭,说明已收集满 C D b
【解析】
(1)根据常用仪器的名称解答;
(2)根据反应物状态和反应条件选择发生装置,反应原理书写文字表达式,排空气法收集的氧气比用排水法收集的氧气干燥解答,氧气性质进行分析解答;
(3)根据装置的特点和反应的原理进行分析解答;
(4)根据二氧化碳的性质进行分析解答;
(5)根据反应物状态和反应条件选择发生装置,乙炔的性质选择收集装置;
(6)根据乙炔的性质进行分析解答。
(1)图中数字②所代表的仪器名称是分液漏斗;
(2)实验室用高锰酸钾制取氧气,反应物的状态是固体,反应的条件是加热,用固体加热型的发生装置,发生装置选B;高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的文字表达式为高锰酸钾![]() 锰酸甲+二氧化锰+氧气;排空气法收集的氧气比用排水法收集的氧气干燥,氧气的密度大于空气,可用向上排空气法收集。收集到一瓶较干燥的氧气来做蜡烛在氧气中燃烧的实验,收集装置应选E;氧气具有助燃性,验证氧气的方法是将带火星的木条伸入集气瓶内,木条复燃,证明是氧气;
锰酸甲+二氧化锰+氧气;排空气法收集的氧气比用排水法收集的氧气干燥,氧气的密度大于空气,可用向上排空气法收集。收集到一瓶较干燥的氧气来做蜡烛在氧气中燃烧的实验,收集装置应选E;氧气具有助燃性,验证氧气的方法是将带火星的木条伸入集气瓶内,木条复燃,证明是氧气;
(3)分液漏斗可利用活塞控制滴液的快慢,控制反应速率,节约药品;过氧化氢在二氧化锰催化作用下分解生成水和氧气,该反应的化学式表达式为H2O2 ![]() H2O + O2;
H2O + O2;
(4)二氧化碳的密度比空气大且能溶于水,所以用向上排空气法收集,收集装置应选择E;二氧化碳不能燃烧也不能支持燃烧,检验二氧化碳是否收集满的方法是把燃着的木条放在集气瓶口,木条熄灭,说明已收集满;
(5)根据“实验室用电石(固体)与水在常温下反应(反应很剧烈)制取乙炔”可知,反应物的状态是固体和液体,在常温下反应,发生装置可选用B和C,该反应很剧烈,为了使反应平稳的进行,需控制反应的速率,制取乙炔应选择的发生装置是C;排水法收集的氧气比用排空气法收集的氧气纯度高,乙炔是不溶于水的气体,收集到较纯净乙炔,可用排水法收集,收集装置可选D;
(6)乙炔密度比空气略小,用万能瓶收集时,应从b管通入。

 阅读快车系列答案
阅读快车系列答案【题目】云通过探究发现,氯酸钾与氧化铜(CuO)、氧化铁(Fe2O3)混合加热,也能较快产生氧气,于是进行如下探究:
(查阅资料)氯酸钾的熔点为356℃,常温下稳定,在400℃以上则分解产生氧气。酒精灯加热温度为400℃~500℃。
(提出猜想)除MnO2、CuO外,Fe2O3也可以作氯酸钾分解的催化剂。
(完成实验)按下表进行实验并测定分解温度。
实验编号 | 实验药品 | 分解温度 |
1 | 3.0g氯酸钾 | 460℃ |
2 | 3.0g氯酸钾和0.5g二氧化锰 | 248℃ |
3 | 3.0g氯酸钾和0.5g氧化铜 | 267℃ |
4 | 3.0g氯酸钾和Xg氧化铁 | 290℃ |
(分析数据,得出结论)
(1)实验3的化学反应式:______________________。
(2)小云从下图中选择该实验的最佳发生装置是__________。
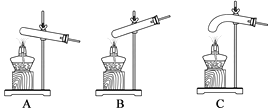
(3)实验4中X的值应为__________,由实验__________与实验4对比,证明猜想合理。
(4)通过实验测得的数据,小云绘出了部分下图,请帮他完成该图。
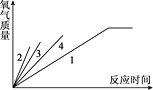
(结论)通过该实验探究中,得到的结论有__________(填序号)。
A.催化剂可降低反应温度
B.二氧化锰只能催化氯酸钾的分解
C.催化剂的质量和性质在反应前后不变
D.催化剂可改变产物的质量
E.三种催化剂中,二氧化锰对氯酸钾分解催化效果最好
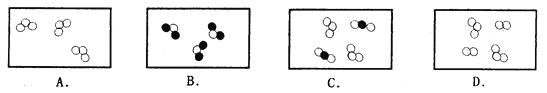
【题目】被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的双氧水(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体。实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体,请填写有关内容:
实验步骤 | 实验现象 | 实验结论 |
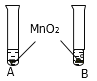
①将等体积的两种无色液体分别加入A、B两个试管中。 ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象。
| A试管中无明显现象 B试管中有气泡产生 | A试管中的无色液体是: _________; B试管中的无色液体是: ________; |
(1)B试管中发生反应的文字表达式:__________
(2)如何验证B试管中产生的气体(写出操作步骤、实验现象和结论)?______。