题目内容
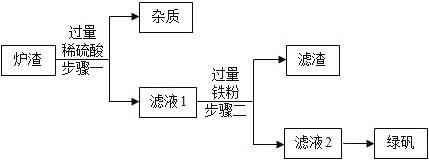
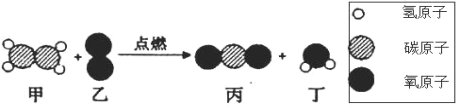
【题目】难溶性杂卤石属于“呆矿”,主要成分有K2SO4、MgSO4、CaSO4、不溶性杂质等(假设杂质不参加反应),为能充分利用钾资源,某工厂用溶浸杂卤石制备硫酸钾,工艺流程如下:
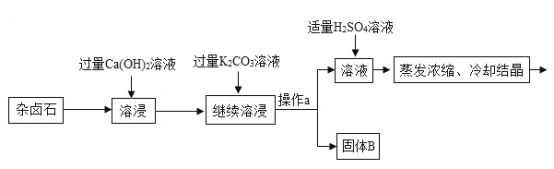
(1)在实验流程中加入过量的Ca(OH)2溶液,目的是出去主要成分中的___;发生反应的化学方程式是___。
(2)操作a的名称是___。
(3)请写出固体B的两种主要成分___、___(用化学式表示)
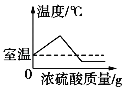
(4)在使用Ca(OH)2溶液和K2CO3溶液对杂卤石进行“溶浸”时,为探究获得较高浸出杂卤石主要成分的浸取率,某实验小组用测得浸取液中K+的质量分数乱来表示浸取率,在相同的时间里,进行了下述实验组:
实验 | 温度/℃ | Ca(OH)2用量/g | K+浸取率/% |
a | 25 | 2.5 | 72.4 |
b | 40 | 2.5 | 86.55 |
c | 40 | 3 | 90.02 |
d | 60 | 3 | 91.98 |
e | 60 | 4 | 91.45 |
①上述实验的数据中,温度与K+浸取率的关系是___。
②上述5组实验中,若要获得最佳的K+浸取率,选择的反应条件是___℃和Ca(OH)2___g。
【答案】MgSO4 MgSO4+Ca(OH)2=Mg(OH)2↓+CaSO4 过滤 Mg(OH)2 CaCO3 温度越高,K+浸取率越高 60 3
【解析】
(1)在实验流程中加入过量的Ca(OH)2溶液,目的是除去主要成分中的MgSO4;
发生反应的化学方程式是:MgSO4+Ca(OH)2=Mg(OH)2↓+CaSO4;
(2)操作a的名称是过滤;
(3)根据流程图可知,氢氧化钙与硫酸镁反应生成氢氧化镁和硫酸钙,过量的碳酸钾溶液与氢氧化钙反应生成碳酸钙和氢氧化钾,固体B的两种主要成分是Mg(OH)2和CaCO3;
(4)①上述实验中,由a和b、c和d可知,温度越高,K+浸取率越高;
②如表5组实验中,d中K+浸取率最高,因此若要获得最佳的K+浸取率,选择的反应条件是60℃和Ca(OH)23g;

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是
A | B | C | D | |
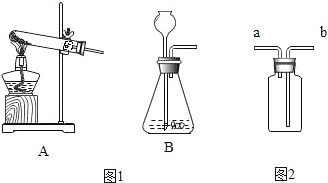
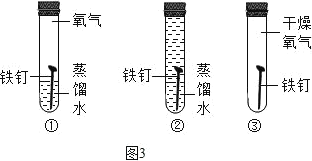
实 验 装 置 |
硫在氧气中燃烧 |
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
|
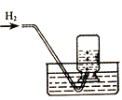
解释 | 集气瓶中的水: 吸收放出的热量 | 量筒中的水: 通过水体积的变化得出O2体积 | 集气瓶中的水: 冷却生成物,防止集气瓶炸裂 | 集气瓶中的水: 水先将集气瓶内的空气排净,后便于观察H2何时收集满 |
A. A B. B C. C D. D