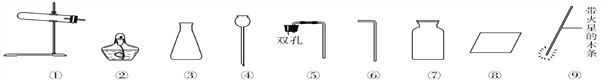
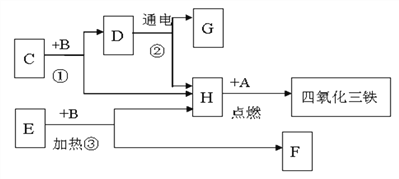
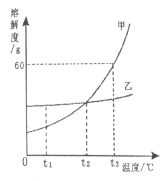
题目内容
【题目】酸与碱之间发生中和反应,其实质是酸溶液中大量自由移动的H+和碱溶液中大量自由移动的OH-结合成水分子的过程。请根据以下氢氧化钠溶液与稀盐酸反应的实验,回答问题。
【实验1】用酚酞试液
(1)向一锥形瓶中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为______色为止,共用去稀盐酸20g,则反应后溶液中溶质质量分数为_________(结果精确到0.1%)。反应后溶液中的溶质可用___________的方法(填一操作名称)使其析出。用酚酞作指示剂可逐滴控制酸、碱溶液反应的量,视觉效果灵敏,操作简便。
【实验2】用pH试纸
(2)向一支试管内倒入约2mL氢氧化钠溶液,再逐滴滴入盐酸,边滴边振荡。然后用玻璃棒蘸取反应液沾到pH试纸上,与标准比色卡对照。因无法通过肉眼观察到反应进程,需间隔数滴多次检测溶液的pH,所以每使用玻璃棒蘸取溶液前,必须进行__________的预处理。
【小 结】
(3)除了用酸碱指示剂、pH试纸外,还可用________________(填方法)检测中和反应是否发生。
【答案】 无 2.9% 蒸发结晶(或蒸发) 洗净并擦干 测温度变化(或用pH计测试或测反应前后溶液导电性)
【解析】氢氧化钠与盐酸反应生成的氯化钠可以通过蒸发的方法使其析出,用PH试纸测定溶液的PH,使用的玻璃棒必须保证洁净,中和反应是放热反应,可以通过测温度的方法检验。
(1)氢氧化钠和盐酸恰好完全反应时溶液呈中性,酚酞恰好变为无色,设生成氯化钠的质量为x,则有
NaOH+HCl= H2O+ NaCl
40 58.5
20g×4.00% x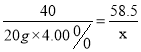
x=1.17g
所以反应后溶液中溶质质量分数为: ![]() ×100%=2.9%,要使氯化钠析出,可以使用蒸发的方法;
×100%=2.9%,要使氯化钠析出,可以使用蒸发的方法;
(2)使用的玻璃棒必须保证洁净,所以本题答案为:洗净并擦干;
(3)中和反应是放热反应,可以通过测温度的方法检验测温度变化。

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案【题目】金属A和非金属B可直接合成化合物AB,甲、乙、丙三人分别做A和B化合反应的实验,充分反应时各人所用A和B的质量不同,但总质量都是9g。甲、乙所用A和B的质量及三人得到化合物AB的质量如下表,请填写表中的空格。
A的用量 | B的用量 | 得到的AB的质量 | |
甲 | 7g | 2g | 6g |
乙 | 4g | 5g | 6g |
丙 | __________ | _________ | 7.5g |