题目内容
【题目】水和溶液对人类的生产、生活具有重要意义。
(1)鉴别硬水和软水常用的试剂是___。
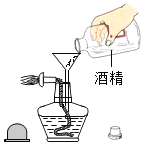
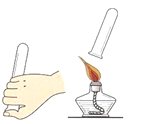
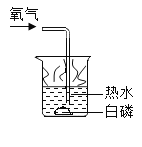
(2)如图是“水中起火”的实验,实验中白磷能在热水中燃烧,热水的作用是:___。写出白磷燃烧的化学方程式___。
(3)将100g溶质质量分数为30%的过氧化氢溶液,稀释为适用于消毒杀菌的3%溶液,需要加水___g。
(4)下表是碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 |
溶解度/g | 12.2 | 21.8 | 39.7 | 53.2 |
①碳酸钠的溶液随温度的变化趋势是____。
②10℃时将112.2g碳酸钠饱和溶液升温到40℃,至少需要加入质量为_____g的碳酸钠,溶液才能达到饱和。
【答案】肥皂水 提供热量,使白磷的温度达到着火点 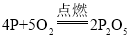 900 碳酸钠的溶解度随温度的升高而增大 41.0
900 碳酸钠的溶解度随温度的升高而增大 41.0
【解析】
(1)常用肥皂水来鉴别硬水和软水,泡沫多的是软水,泡沫少的是硬水;
(2)热水的作用是提供热量,使白磷的温度达到着火点;白磷和氧气反应生成物是五氧化二磷,化学方程式为: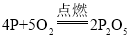 ;
;
(3)稀释前后溶质质量不变,设加水的质量为x,则:![]() ,x=900g,故需要加水900g;
,x=900g,故需要加水900g;
(4)根据表中数值变化可知碳酸钠的溶解度随温度的升高而增大;10℃时,碳酸钠的溶解度为12.2g,则112.2g碳酸钠饱和溶液中碳酸钠的质量为12.2g,溶剂水的质量为100g;40℃时,碳酸钠的溶解度是53.2g,若要使溶液重新达到饱和状态,需要加入碳酸钠质量为53.2g﹣12.2g=41.0g。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】下表列出了KNO3在不同温度下的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(1)由上表可推出KNO3溶解度曲线的变化规律是______。
(2)20℃时,把40gKNO3放入小烧杯中,然后再加100g水不断搅拌,形成溶液的质量为____g;该溶液是___(填“饱和”或“不饱和”)溶液。
(3)如图所示,把上述(2)中的小烧杯放到盛水的大烧杯中。若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,能够使小烧杯中的KNO3溶液溶质的质量分数增大的是____(填序号)。
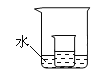
①浓硫酸 ②硝酸铵 ③氢氧化钠 ④冰