题目内容
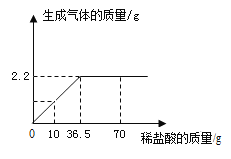
【题目】某学习小组在实验室中用加热氯酸钾和二氧化锰混合物的方法制取氧气,现取氯酸钾和二氧化锰固体混合物60g充分加热,使之完全反应,反应过程中产生气体质量变化如图所示。
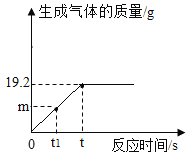
(1)可制得氧气的质量是_____g。
(2)原混合物中氯酸钾的质量是多少?_____(写 出计算过程)
(3)加热至t1时刻,测得固体混合物中二氧化锰的质量分数为22%,则此时生成氧气的质量(m)为_____g。
【答案】19.2 49g 10
【解析】
解:(1)由图像可知:制得氧气的质量为19.2g;
(2)设:原混合物中氯酸钾的质量为x。
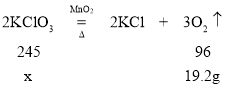
![]() x=49g
x=49g
原混合物中氯酸钾的质量为49g;
则二氧化锰的质量为60g-49g=11g;
(3)加热至t1时刻,测得固体混合物中二氧化锰的质量分数为22%,则此时剩余固体混合物的总质量为![]() ,生成氧气的质量=60g-50g=10g。
,生成氧气的质量=60g-50g=10g。

练习册系列答案
相关题目
【题目】在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的说法正确的是( )
物 质 | X | Y | Z | W |
反应前的质量(g) | 2 | 1 | 16 | 16 |
反应后的质量(g) | 12 | m | 8 | 14 |
A.物质Y一定是该反应的催化剂
B.该反应的基本类型为分解反应
C.参加反应的Z与W的质量比为4:1
D.反应后生成X的质量为12 g