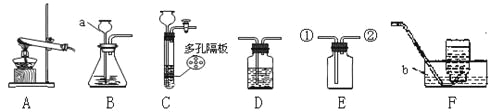
题目内容
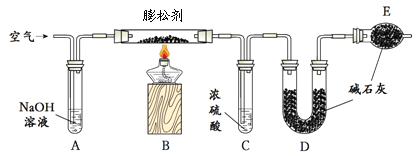
【题目】(2分)最近有科学家提出“绿色自由”构想:将空气吹入K2C03溶液生成KHC03,然后加热使KHC03分解出C02,再转化为有机物实施碳循环。根据以下流程回答。
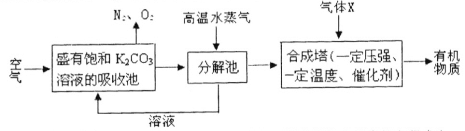
(1)吸收池中主要发生K2C03+H20+C02=2KHC03,则分解池中反应的方程式为 ;
(2)在合成塔中若气体X是H2,反应生成甲醇(CH3OH)和水,该反应方程式 。
【答案】(1)2KHCO3 = K2CO3+H2O+CO2↑ (2)2CO2+6H2 = 2CH3OH+2H2O
【解析】
试题分析:根据流程图(1)吸收池中主要发生K2C03+H20+C02=2KHC03,则分解池中反应的方程式为2KHCO3 = K2CO3+H2O+CO2↑ (2)在合成塔中若气体X是H2,反应生成甲醇(CH3OH)和水,该反应方程式2CO2+6H2 = 2CH3OH+2H2O.

【题目】(8分)石灰石有许多重要的用途。
(1)以石灰石为原料,可以生产生石灰,生石灰可做干燥剂,某化学兴趣小组的同学对食品厂某批次包装完整、粉状的生石灰成分进行质量检测。
【提出问题】该批次的生石灰成分及含量是否与标签相符?
(标签如图所示)

【猜想与假设】固体成分为:
A:全部是碳酸钙和杂质 B:既有碳酸钙,也有氧化钙和杂质
C:全部是 和杂质。
【设计并完成实验】
实验操作 | 实验现象 | 实验结论 |
第一步操作:取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有 |
第二步操作:再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有 |
【实验结论】该兴趣小组同学得出的结论:剩余固体成分与【猜想与
假设】中的 (填A、B或C)相同。
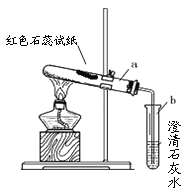
【定量测定】称取10克该批次的生石灰样品,置于锥形瓶中,向其中缓慢加稀盐酸,直至无气泡产生,电子天平读数变小0.88克,将锥形瓶中残留物进行过滤、洗涤、干燥,得到固体质量为0.2克。

【问题讨论】由于生石灰与酸反应放出热量,导致水蒸气随CO2一起从导管口逸出,这一因素使测得的生石灰的最终含量将 (选填“偏小”“偏大”或“无影响”)。反应生成的CO2也会代替原有的空气残留在锥形瓶中,这一因素对测定结果也有影响。
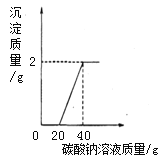
(2)实验小组的同学对实验室制取二氧化碳反应后的溶液进行了如下探究:
取大理石和盐酸反应且过滤后所得废液20克于烧杯中,逐滴滴入碳酸钠溶液至过量,滴入碳酸钠溶液的质量与生成沉淀的质量的变化关系如图所示。请根据图中信息计算废液中氯化钙的质量分数是多少?(写出计算过程)