题目内容
【题目】研究和控制化学反应条件有重要意义。
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间。
实验 | 30%双氧水的质量(g) | 加入的谁的体积(mL) | 二氧化锰质量 | 收集时间(s) |
① | 10 | 40 | 5 | 200 |
② | 20 | 30 | 5 | 100 |
③ | 30 | 20 | 67 |
①实验时,取用二氧化锰的仪器是(填仪器名称)。
②如下图所示,发生装置应选用(填编号,下同),此题中气体收集装置应采用的是。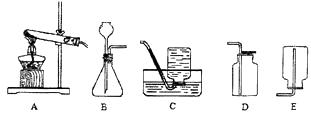
③实验3中,加入的二氧化锰质量为g。
④相同条件下,实验3产生氧气的速率最快,说明。
⑤第三次实验结束后,测得容器中全部剩余物的总质量为50.8g,则该实验生成氧气的质量是g。
(2)二氧化碳与水反应,在常温下进行的化学方程式为 , 在叶绿素、光照的条件下发生光合作用生成葡萄糖 (C6H12O6)和氧气的化学方程式为 , 反应物相同,但产物不同。说明不同,产物不同。
【答案】
(1)药匙或纸槽,B,C或D,5g,双氧水的浓度越大,反应速率越快,4.2g
(2)CO2+H2O=H2CO3,6CO2+6H2O ![]() C6H12O6+6O2,反应条件
C6H12O6+6O2,反应条件
【解析】( 1 ) ①取粉末状药品应该用药匙或纸槽;加热固体制取气体,发生装置为A,固体和液体常温下反应制取气体应选用的发生装置为B;氧气的密度比空气的大,可以用向上排空气法收集,氧气难溶于水可以用排水法收集。据化学反应中的控制变量的原则,实验3中,加入的二氧化锰质量为5g;由表格中数据可知双氧水的浓度越大,反应速率越快;据质量守恒定律可知,反应前后物质的总质量不变,所以该实验生成氧气的质量55g-50.8g= 4.2g;(2)二氧化碳与水反应,在常温下进行反应,生成碳酸,化学方程式为CO2+H2O=H2CO3 ;在叶绿素、光照的条件下发生光合作用生成葡萄糖 (C6H12O6)和氧气的化学方程式为 6CO2+6H2O ![]() C6H12O6+6O2 ;由此可知反应物相同,但由于反应条件不同,产物不同。
C6H12O6+6O2 ;由此可知反应物相同,但由于反应条件不同,产物不同。
所以答案是:(1)药匙或纸槽;B;C或D;5g;双氧水的浓度越大,反应速率越快; 4.2g;(2)CO2+H2O=H2CO3 ;6CO2+6H2O ![]() C6H12O6+6O2 ;反应条件。
C6H12O6+6O2 ;反应条件。
【考点精析】利用书写化学方程式、文字表达式、电离方程式对题目进行判断即可得到答案,需要熟知注意:a、配平 b、条件 c、箭号.