题目内容
【题目】将一定质量的NaCl和Na2SO4固体混合物完全溶于水后,加入一定质量分数的BaCl2溶液208g,恰好完全反应,过滤,得到23.3g沉淀,经测定滤液中含氯元素的质量为21.3g(不考虑过滤过程中物质质量的损失)。计算:(1)所加BaCl2溶液的溶质质量分数。
(2)原固体混合物中Na2SO4的质量。(3)原固体混合物中NaCl的质量
【答案】(1)10﹪ (2)14.2 (3)23.4
【解析】有题可知生成硫酸钡的质量是23.3g,根据化学方程式列比例求出Na2SO4的质量,BaCl2的质量,由化学式求出BaCl2中氯元素的质量,可得出原固体混合物中NaCl中氯元素的质量,从而求得NaCl的质量
解:设BaCl2的质量是xg,Na2SO4的质量是yg,
Na2SO4+BaCl2=2NaCl+BaSO4↓
142 208 233
y x 23.3g
142/y=208/x=233/23.3g
X=14.2g,y=20.8g
BaCl2溶液的溶质质量分数=![]() =10﹪
=10﹪
BaCl2中氯元素的质量=![]() g=7.1g
g=7.1g
原固体混合物中NaCl中氯元素的质量=21.3g-7.1g=14.2g
原固体混合物中NaCl的质量=14.2g![]() =23.4g
=23.4g

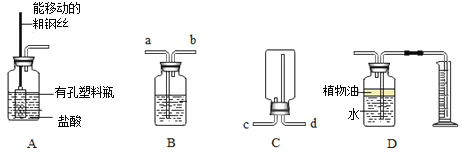
【题目】同学们在学习碱的化学性质时,进行了如图所示的实验。
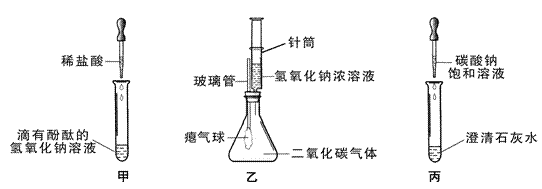
(1)写出甲实验中盐酸和氢氧化钠反应的化学方程式_________。
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是_________。
(3)丙实验中观察到试管内有白色沉淀产生。
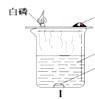
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问。
【提出问题】 废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、水和________(写物质名称)。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有如下猜想。
小云认为:只有碳酸钠 小红认为:只有氢氧化钙 小林认为:是氢氧化钠和碳酸钠
你认为还可能是___________(写一种猜想)
【实验设计】请你设计实验证明小林的猜想正确,把下面表格填写完整即可。
实验操作 | 实验现象 | 实验结论 |
取少量废液缸中上层清液于试管中,加入___,静置。 | _____________。 | 小林的猜想正确 |
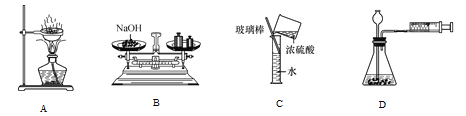
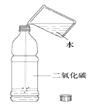
【题目】分类、类比是学习化学常用的方法。
(1)初中化学有许多实验,若按照实验方法分类,则应将实验中的A与______(填B、C、D),归为一类,依据______________________________。
|
|
|
|
A | B | C | D |
(2)“炔”代表的是一类有机物,其中乙炔C2H2俗称风煤和电石气,是炔烃化合物系列中体积最小的一员,炔烃的书写是有一定规律的,例如:丙炔C3H4,丁炔C4H6,根据以上规律写出戊炔的化学式____________,戊炔燃烧的产物是______________。