题目内容
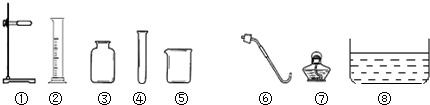
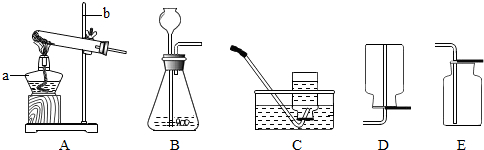
 过氧化氢(H2O2)溶液在Mn02作催化剂的条件下,能迅速发生分解.分液漏斗可以通过调节活塞控制液体的滴加速率.现欲制取干燥且纯净的氧气,采用如图所示的装置.回答下列问题:
过氧化氢(H2O2)溶液在Mn02作催化剂的条件下,能迅速发生分解.分液漏斗可以通过调节活塞控制液体的滴加速率.现欲制取干燥且纯净的氧气,采用如图所示的装置.回答下列问题:(1)分液漏斗中盛放的物质是
双氧水
双氧水
.(2)装置B中的药品是
生石灰
生石灰
.(3)A中发生反应的化学方程式是
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
;检验C中集满氧气的方法是
| ||
把带火星的木条放在集气瓶口看是否复燃
把带火星的木条放在集气瓶口看是否复燃
.(4)该实验与用加热KMnO4制取O2的实验相比,其优点是
②④
②④
(填序号).①生成物只有氧气 ②不需加热 ③生成氧气多 ④易控制反应速率
(5)若改变装置A中的药品,此套装置还可以用来制取
CO2
CO2
气体,反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.分析:本题考查对实验室制取氧气两种方法的比较及气体的干燥.特别注意两种方法的反应原理使用固体生石灰作干燥剂,排空气法收集氧气.
解答:解:(1)分液漏斗应加入液体物质:过氧化氢溶液 或 双氧水,锥形瓶里应先放人固体物质:二氧化锰 或 MnO2;
(2)装置B中的药品是干燥剂生石灰,
(3)A中反应,双氧水在二氧化锰作用下生成水和氧气,化学方程式为:2H2O2
2H2O+O2↑,检验C中集满氧气的方法是把带火星的木条放在集气瓶口看是否复燃;
(4)该实验与用加热KMnO4制取O2的实验相比,其优点是不需加热、易控制反应速率
(5)若改变装置A中的药品,此套装置还可以用来制取CO2;反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑
答案是:(1)双氧水(2)生石灰(3)2H2O2
2H2O+O2↑;把带火星的木条放在集气瓶口看是否复燃;(4)②④(5)CO2;CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)装置B中的药品是干燥剂生石灰,
(3)A中反应,双氧水在二氧化锰作用下生成水和氧气,化学方程式为:2H2O2
| ||
(4)该实验与用加热KMnO4制取O2的实验相比,其优点是不需加热、易控制反应速率
(5)若改变装置A中的药品,此套装置还可以用来制取CO2;反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑
答案是:(1)双氧水(2)生石灰(3)2H2O2
| ||
点评:本题主要考查气体制备原理和操作方法、步骤及注意事项,运用所学化学知识综合分析和解决实际问题的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目
 实验室中常用高锰酸钾受热分解制取氧气.
实验室中常用高锰酸钾受热分解制取氧气.