题目内容
【题目】化学基础与常识
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);

A电缆 B.电热壶 C.金属丝 D.金属乐器
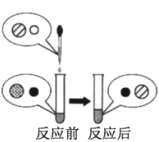
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“○”“![]() ”“●”“
”“●”“ ![]() ”表示不同离子)。则“○”与“
”表示不同离子)。则“○”与“![]() ”反应生成了_________(填物质名称)。
”反应生成了_________(填物质名称)。
(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。

写出反应I中,发生反应的化学方程式:_____________________________。
【答案】 B 水 CaF2 SO2+I2+2H2O=H2SO4+2HI
【解析】(1) A、电缆是利用金属的导电性,故错误;B、电热壶利用金属的导热性,故正确;C、金属丝利用金属的延展性,故错误;D、金属乐器利用金属具有金属光泽、硬度大,故错误;(2) 氢氧化钠与稀盐酸反应生成氯化钠和水,中和反应的实质是氢离子和氢氧根离子结合生成水分子;(3)在化学反应CaSiO3+6HF=X+SiF4↑+3H2O中,反应前后原子的数目、种类都不变;反应前有6个氢原子、6个氟原子、1个硅原子、3个氧原子、1个钙原子;反应后除X外有6个氟原子、1个硅原子、6个氢原子、3个氧原子,因此每个X分子中应该有2个氟原子和1个钙原子,故X的化学式为CaF2;(4)据图可知,反应I中是由SO2、I2和2H2O生成H2SO4和2HI,反应的化学方程式:SO2+I2+2H2O=H2SO4+2HI。

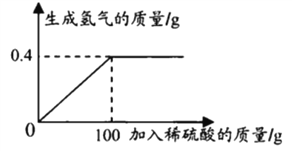
【题目】小华有一只银手镯(银锌合金),她想用实验探究手镯中银的含量。先用电子秤称得手镯的质量是25.00克,再用稀盐酸分多次与此手镯充分反应。实验数据如下表:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入烯盐酸的质量(克) | 10.00 | 10.00 | 10.00 | 10.00 | 10.00 |
充分反应后剩余固体的质量(克) | 24.35 | 23.70 | 23.05 | 23.00 | 23.00 |
根据上表中数据分析,完成下列问题:
(1)手镯中银的质量是________克。
(2)所用稀盐酸中溶质的质量分数是多少________?
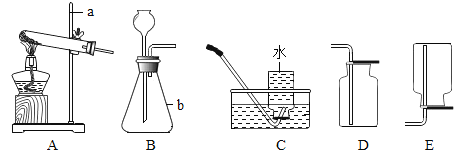
【题目】在高温条件下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小莉很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
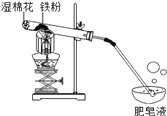
(1)试管尾部放一团湿棉花的目的是_____________________。
(2)探究生成的气体是什么?
用燃着的木条靠近飘到空中的肥皂泡,
有爆鸣声。说明生成的气体是_______。
(3)探究试管中剩余固体成分是什么?
【查阅资料】(1)常见铁的氧化物的物理性质如下表:
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
(2)稀盐酸(或稀硫酸)与铁反应产生气体,与铁的氧化物反应没有气体产生。
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是_____________。
【实验探究】根据猜想与假设,设计实验方案加以检验。
实验操作 | 实验现象 | 实验结论 |
____________________ | _________ | 剩余固体是Fe3O4 |
【实验结论】铁和水蒸气反应的化学方程式为____________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是___________________。