题目内容
【题目】某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示。
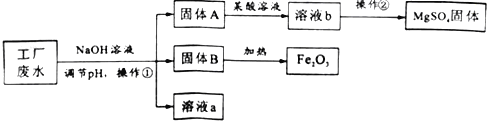
(1)固体A与某酸反应的化学方程式为____________。操作②时,当__________即可停止加热。
(2)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为__________。
(3)溶液a除了可能含有NaOH外,还一定含有的溶质是_____________(填化学式)。
【答案】 Mg(OH)2+H2SO4=MgSO4+2H2O 少量水(或析出大量晶体) H2O NaCl、Na2SO4
【解析】本题考查了酸、碱、盐的化学性质,混合物的分离等。根据物质的性质以及物质间的反应,结合化学方程式的书写的知识进行分析解答。
工业废水加入氢氧化钠溶液,会与硫酸镁反应生成氢氧化镁沉淀和硫酸钠,与氯化铁反应生成氢氧化铁沉淀和氯化钠,A中加入某酸后得到硫酸镁,则加入的酸是硫酸,固体A是氢氧化镁;固体B加热得到的是氧化铁, 则B是氢氧化铁,溶液a中含有生成的氯化钠和硫酸钠。因此:
(1)固体A与某酸反应是氢氧化镁与硫酸的反应,生成的是硫酸镁和水,反应的化学方程式为Mg(OH)2+H2SO4=MgSO4+2H2O;操作②是蒸发操作,当还有少量水(或析出大量晶体)时停止加热;
(2)固体B是氢氧化铁,加热的产物是两种常见氧化物,一种是氧化铁,根据质量守恒定律可知,另一种氧化物是水,化学式是H2O;
(3)溶液a中含有生成的氯化钠和硫酸钠,化学式分别是NaCl、Na2SO4。

 名校课堂系列答案
名校课堂系列答案【题目】对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
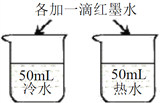
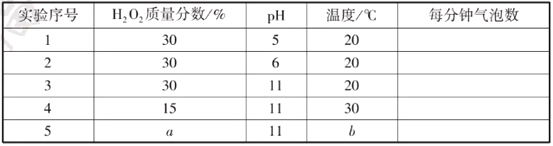
A | 探究温度对分子运动快慢的影响 |
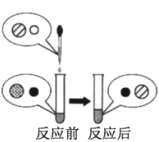
| B | 探究水对铁钉锈蚀的影响 |
|
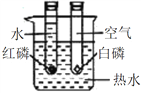
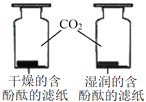
C | 探究空气是燃烧的必要条件 |
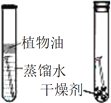
| D | 探究CO2与水反生反应 |
|
A. A B. B C. C D. D
【题目】实验室中分别用高锰酸钾、过氧化氢、氯酸钾制取比较纯净的氧气。请你按照要求回答问题:
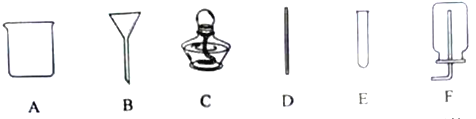
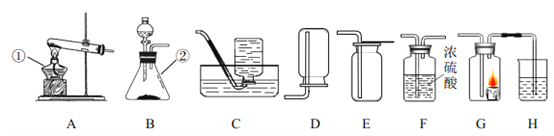
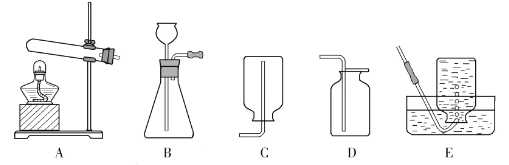
(l)结合下图所提供装置完成下列表格
反应物 填写内容 | 化学方程式 | 气体制取装置 组合(填序号) |
高锰酸钾 | 例:2KMnO4 | ____________ |
过氧化氧(二氧化锰) | ___________________________________ | ____________ |
氯酸钾(二氧化锰) | ___________________________________ |
|
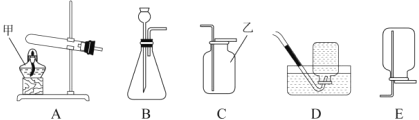
(2)请结合上图回答问题:
①写出甲、乙所指仪器名称:甲_______________;乙_______________;
②用过氧化氢制氧气的装置与其他两种方法的装置相比具有的优点____________,_____________(写出两条);
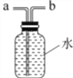
③若用下图装置收集一瓶氧气,气体应从____(填a或b)端进入集气瓶。