题目内容
【题目】根据下列实验装置图,回答有关问题。
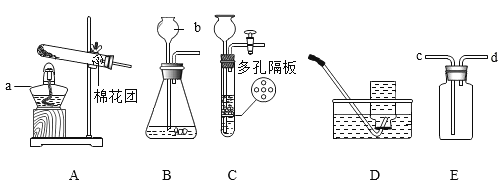
(1)仪器b的名称为______。
(2)若实验室要加热KMnO4,制取较纯净的氧气,选择的装置组合是____,反应的化学方程式为______。
(3)与B相比,C作为发生装置的优点是____。如用装置E收集二氧化碳气体,气体应___从(填“c”或 “d”)端通入,此时检验二氧化碳气体收集满的方法是_____。
(4)某化学兴趣小组利用“数字化实验”装置探究CO2的相关反应,先后将针筒内的溶液快速全部推入至充满CO2的三颈烧瓶中,测得一段时间内压强变化如图所示


①ab段反应的化学方程式为_______。
②bc段压强不变,原因是_________________。
③导致cd段压强变化的实验操作是________。
④cd段气压变化的原因是___________。(填序号)。
a 三颈烧瓶内的二氧化碳气体被消耗
b 三颈烧瓶内又产生了二氧化碳气体
c 三颈烧瓶内氢氧化钠与盐酸发生了反应
【答案】长颈漏斗 AD ![]() 可控制反应的发生和停止 c 燃着的木条放在d管口,燃着的木条熄灭说明已满
可控制反应的发生和停止 c 燃着的木条放在d管口,燃着的木条熄灭说明已满 ![]() 氢氧化钠溶液与二氧化碳充分反应后,反应停止,且加入稀盐酸后,稀盐酸先与未反应的氢氧化钠反应生成氯化钠和水,瓶中气体体积无明显变化 向三颈烧瓶中推入盐酸 b
氢氧化钠溶液与二氧化碳充分反应后,反应停止,且加入稀盐酸后,稀盐酸先与未反应的氢氧化钠反应生成氯化钠和水,瓶中气体体积无明显变化 向三颈烧瓶中推入盐酸 b
【解析】
(1)仪器b的名称为长颈漏斗;
(2)实验室加热高锰酸钾制取氧气,该反应属于固体加热反应,发生装置应选A;氧气不易溶于水,密度比空气略大,选择的装置组合是:AD;高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气,该反应的化学方程式为:![]() ;
;
(3)与B相比,C作为发生装置的优点是:可以控制反应的发生和停止。以石灰石和稀盐酸反应为例,将石灰石置于多孔隔板上,打开止水夹,通过长颈漏斗添加稀盐酸,使固液接触,反应发生,产生气体;关闭止水夹,装置内压强增大,将稀盐酸压回长颈漏斗中,固液分离,反应停止。二氧化碳的密度比空气大,如用装置E收集二氧化碳气体,气体应从c端通入;此时检验二氧化碳的方法:将燃着的木条放在d端管口,木条熄灭,说明已经集满;
(4)①由图可知,ab段压强逐渐减小,原因是氢氧化钠能与二氧化碳反应生成碳酸钠和水,消耗二氧化碳,使装置内压强减小,该反应的化学方程式为:![]() ;
;
②三颈烧瓶中,氢氧化钠与二氧化碳完全反应后,反应停止,气体体积不变,瓶中压强不变,且加入稀盐酸后,稀盐酸先与未反应的氢氧化钠反应,无气体生成,瓶中压强也不会明显改变,故bc段压强不变的原因是:氢氧化钠溶液与二氧化碳充分反应后,反应停止,且加入稀盐酸后,稀盐酸先与未反应的氢氧化钠反应生成氯化钠和水,瓶中气体体积无明显变化;
③氢氧化钠与二氧化碳反应生成碳酸钠和水,待氢氧化钠与二氧化碳完全反应后,推入稀盐酸,碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,有气体生成,压强增大。故导致cd段压强变化的实验操作是:向三颈烧瓶中推入盐酸;
④由③的分析可知,推入稀盐酸后,碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,有气体生成,压强增大。故cd段气压变化的原因是:b。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表。下列说法错误的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前物质的质量(g) | 8 | 32 | 5 | 4 |
反应后物质的质量(g) | 16 | X | 5 | 24 |
A. 该反应为分解反应
B. 丙可能是该反应的催化剂
C. 甲、丁两物质反应前后质量变化之比为2:5
D. X值为28
【题目】将“曼妥思”糖投入碳酸饮料瓶中,会产生大量气泡并带着饮料从瓶口喷出,形成一定高度的“喷泉”。这是由于瓶内气压增大造成的。

[提出问题]瓶内气压增大与什么有关?
[进行实验]
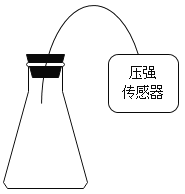
实验1: 25°C时,将“曼妥思”与50mL碳酸饮料混合,利用压强传感器测量从0s至60s时增大的压强值( 装置如图)。
实验序号 | 1-1 | 1-2 | 1-3 | 1-4 | 1-5 | 1-6 |
“曼妥思”数目/颗 | 1 | 2 | 3 | 4 | 5 | 6 |
60s时增大的压强值/kPa | 3.91 | 6.19 | 6.53 | 7.42 | 8.67 | 10.60 |
实验2:将“曼妥思”与50mL碳酸饮料混合,利用压强传感器测量从0s至60s时增大的压强值。
实验序号 | “曼妥思”数目/颗 | “曼妥思”形状 | 温度/°C | 60s时增大的压强值/kPa |
2-1 | 4 | 每颗切成4等份 | 25 | 10.67 |
2-2 | 4 | 每颗切成4等份 | 37 | 18.75 |
2-3 | 4 | 每颗研碎成粉末 | 37 | 23.58 |
2-4 | 6 | 每颗切成4等份 | 25 | 13.86 |
2-5 | 6 | 每颗研碎成粉末 | 25 | 20.57 |
2-6 | 6 | 每颗研碎成粉末 | 37 | 25.46 |
[解释与结论]
(1) “曼妥思”与碳酸饮料混合后产生的气体能使澄清石灰水变浑浊,该气体为______________。
(2)实验1的目的是______________。
(3)通过对比实验2中____________(填实验序号)可知“曼妥思” 形状会影响60s时增大的压强值。
(4)实验2-3的压强值大于实验2-5的原因是______________。
[反思与评价]
(5)相同条件下, “曼妥思”研碎后,测得压强值较大的原因是______________。
(6)依据实验2分析,用“曼妥思”和碳酸饮料进行“喷泉”实验,为形成明显效果最好选择37°C、50mL碳酸饮料和______________。
【题目】皮蛋又称松花蛋,因其风味独特,深受人们喜爱。某兴趣小组在市场上获得了少许腌制皮蛋的原料。拿到实验室进行实验。将该固体混合物放于烧杯中,缓慢加入足量的蒸馏水,充分溶解后过滤,得到白色沉淀A和无色澄清滤液B。
[提出问题](1)白色沉淀A是什么? (2)无色滤液B中的溶质有哪些?
[查阅资料]腌制皮蛋的原料配方是少量NaCl、CaO和过量Na2CO3的固体混合物。
[理论推理](1)白色沉淀A是CaCO3,请写出生成该沉淀的化学方程式:_________。
(2)滤液B中含有Na2CO3、NaOH、NaCl三种溶质。
[实验验证]为证明滤液B中存在的三种溶质,同学们进行了如下实验。
步骤 | 实验操作 | 实验现象 | 实验结论 |
Ⅰ | 取少量滤液B于试管中,加入过量的Ba(NO3)2溶液,过滤 | ____ | 滤液B中含有Na2CO3、NaOH、NaCl. |
Ⅱ | 取少量步骤I中所得滤液于试管中,加入酚酞溶液 | ____ | |
Ⅲ | 另取少量步骤I中所得滤液于试管中,先加入足量的稀硝酸,再加入_____溶液 | 产生白色沉淀 |
[拓展提升] (1)向步骤I中加入过量Ba(NO3)2溶液的目的是_______。
(2)小妮同学认为若将步骤I中的Ba(NO3)2溶液换为BaCl2溶液,进行以上实验,最终也能证明滤液B中存在的三种溶质。你认为该方案是否合理并说出理由________。
(3)小轩同学认为向滤液B中先加入酚酞溶液,后加入过量的Ba(NO3)2溶液,也能得出滤液B的溶质中含有Na2CO3和NaOH的结论,大家都同意他的观点,理由是__________。