题目内容
实验室中现有一种固体混合物,其中可能含有Cu、CuO、Na2CO3、NaOH六种物质中的两种或多种.按下图所示进行实验,出现的现象如图中所述.
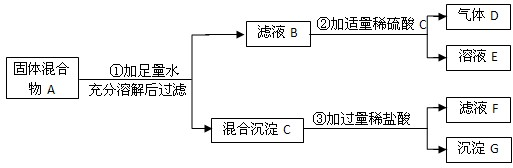
试根据实验过程和发生的现象判断:
(1)气体D是(写化学式)
(2)若滤液F呈蓝色,则滤液F中一定存在的溶质是(写化学式)
(3)写出过程③中发生的化学反应的化学方程式
(4)混合物A中,一定存在的物质是(写化学式)

试根据实验过程和发生的现象判断:
(1)气体D是(写化学式)
CO2
CO2
.(2)若滤液F呈蓝色,则滤液F中一定存在的溶质是(写化学式)
CuCl2、HCl
CuCl2、HCl
.(3)写出过程③中发生的化学反应的化学方程式
CuO+2HCl=CuCl2+H2O
CuO+2HCl=CuCl2+H2O
.(4)混合物A中,一定存在的物质是(写化学式)
Na2CO3、Cu、CuO
Na2CO3、Cu、CuO
.分析:固体混合物加入水后得到沉淀C,向C中加入稀盐酸后生成蓝色溶液,说明在沉淀中有氧化铜,但是仍有沉淀G,从所给的物质可以判断出该沉淀应该为铜;对于滤液B加入稀硫酸后生成了气体,说明存在着碳酸钠,同时可以排除氯化钡的存在,可以据此答题.
解答:解:(1)向滤液B中加入稀硫酸产生了气体D,分析所给的物质,能与酸反应产生气体的物质是碳酸盐,所以产生的气体是CO2;
(2)向C中加入稀盐酸后生成蓝色溶液,说明在沉淀中有氧化铜,蓝色是由于氯化铜溶液体现的,另外由于盐酸过量,所以滤液F的溶质是氯化铜和氯化氢;
(3)由以上的分析可知反应③是氧化铜与盐酸的反应,其方程式为:CuO+2HCl=CuCl2+H2O;
(4)最后还有不溶物存在,说明有不与稀盐酸反应的物质,分析所给的几种物质,铜不与稀盐酸反应,所以一定含铜,根据(1)的分析可知一定含碳酸钠,因此混合物A中含有的物质是:Na2CO3、Cu、CuO,可能含有氢氧化钠;
故答案为:(1)CO2;
(2)CuCl2、HCl;
(3)CuO+2HCl=CuCl2+H2O;
(4)Na2CO3、Cu、CuO;
(2)向C中加入稀盐酸后生成蓝色溶液,说明在沉淀中有氧化铜,蓝色是由于氯化铜溶液体现的,另外由于盐酸过量,所以滤液F的溶质是氯化铜和氯化氢;
(3)由以上的分析可知反应③是氧化铜与盐酸的反应,其方程式为:CuO+2HCl=CuCl2+H2O;
(4)最后还有不溶物存在,说明有不与稀盐酸反应的物质,分析所给的几种物质,铜不与稀盐酸反应,所以一定含铜,根据(1)的分析可知一定含碳酸钠,因此混合物A中含有的物质是:Na2CO3、Cu、CuO,可能含有氢氧化钠;
故答案为:(1)CO2;
(2)CuCl2、HCl;
(3)CuO+2HCl=CuCl2+H2O;
(4)Na2CO3、Cu、CuO;
点评:解决此类框图式物质推断题时,要根据酸碱盐物质间的复分解反应,结合各物质间反应的实验现象,对此题做出合理的判断,所以要求同学们在平时的学习中要加强知识的储备.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



