题目内容
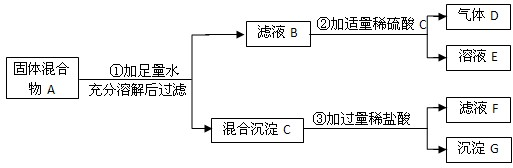
实验室中现有一种固体混合物,其中可能含有Fe2O3、BaSO4、Na2CO3、CaCl2 四种物质中的两种或多种.按图所示进行实验,出现的现象如图中所述(设过程中所有可能发生的反应均恰好完全反应).
试判断:
(1)产生的气体D是(写化学式)
(2)黄色溶液F中一定存在的溶质是(写化学式)
(3)混合物A中,一定不存在的物质是(写化学式)
(4)写出过程③中发生的化学反应方程式:

试判断:
(1)产生的气体D是(写化学式)
CO2
CO2
.(2)黄色溶液F中一定存在的溶质是(写化学式)
FeCl3、HCl
FeCl3、HCl
.(3)混合物A中,一定不存在的物质是(写化学式)
CaCl2
CaCl2
;(4)写出过程③中发生的化学反应方程式:
2Fe2O3+6HCl═2FeCl3+3H2O
2Fe2O3+6HCl═2FeCl3+3H2O
.分析:本题属于推断题,根据题目给出的流程图和信息:Fe2O3、BaSO4都不溶于水,Na2CO3、CaCl2不能共存,滤液B中加入适量的硫酸生成气体,则说明固体中含有碳酸盐,因此A中一定有碳酸钠,那么一定没有氯化钙;沉淀C中加入稀盐酸有黄色溶液出现,则说明固体中含有氧化铁,反应后还有沉底,说明沉淀中一定有硫酸钡,据此解答即可;
解答:解:Fe2O3、BaSO4都不溶于水,Na2CO3、CaCl2不能共存,滤液B中加入适量的硫酸生成气体,则说明固体中含有碳酸盐,因此A中一定有碳酸钠,生成的气体是二氧化碳,那么固体中一定没有氯化钙;沉淀C中加入稀盐酸有黄色溶液出现,因此滤液F中一定有铁离子,则说明固体中含有氧化铁,反应后还有沉淀,说明沉淀中一定有硫酸钡;
(1)由分析知产生的气体D是二氧化碳,化学式为CO2;
(2)黄色溶液中一定含有氧化铁和盐酸反应生成的氯化铁以及过量的盐酸,所以含有的溶质FeCl3、HCl;
(3)由分析知固体中一定不会含有CaCl2;
(4)③是氧化铁与盐酸的反应,方程式为2Fe2O3+6HCl═2FeCl3+3H2O;
故答案为:(1)CO2;(2)FeCl3、HCl;(3)CaCl2;(4)2Fe2O3+6HCl═2FeCl3+3H2O;
(1)由分析知产生的气体D是二氧化碳,化学式为CO2;
(2)黄色溶液中一定含有氧化铁和盐酸反应生成的氯化铁以及过量的盐酸,所以含有的溶质FeCl3、HCl;
(3)由分析知固体中一定不会含有CaCl2;
(4)③是氧化铁与盐酸的反应,方程式为2Fe2O3+6HCl═2FeCl3+3H2O;
故答案为:(1)CO2;(2)FeCl3、HCl;(3)CaCl2;(4)2Fe2O3+6HCl═2FeCl3+3H2O;
点评:此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.

练习册系列答案
相关题目