题目内容
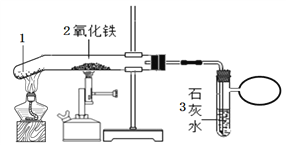
【题目】在研究酸和碱的化学性质时,某小组同学想证明稀盐酸和氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,如下图,试与他们一起完成实验,并得出有关结论。
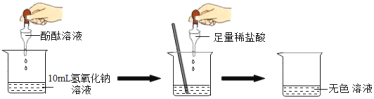
(1)探究稀盐酸和氢氧化钠溶液的反应:
当滴入几滴酚酞试液后,溶液由无色变为_____色。根据上述实验中颜色变化,可确定稀盐酸和氢氧化钠溶液发生了化学反应,反应的化学方程式为_____。
(2)探究上述稀盐酸和氢氧化钠溶液反应后烧杯中的盐酸是否过量:
根据上述图示反应最后烧杯中为无色溶液,不能确定稀盐酸是否过量。同学们又分别选取硝酸银溶液、紫色石蕊试液设计实验方案,请你判断并
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的硝酸银溶液 | 出现白色沉淀 | 稀盐酸过量 |
方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀盐酸过量 |
在上述设计的实验方案中,正确的是_____(填“方案一”或“方案二”),另外一个实验方案错误的原因是_____。
(3)若请你再设计一个确定稀盐酸是否过量的实验方案,你选用的药品是_____。
【答案】红 NaOH+HCl=NaCl+H2O 方案二 氢氧化钠和盐酸反应后生成的氯化钠也能和硝酸银反应生成白色沉淀氯化银 锌粒(合理即可)
【解析】
(1)探究稀盐酸和氢氧化钠溶液的反应:
当滴入几滴酚酞试液至氢氧化钠中后,溶液由无色变为红色;滴加稀盐酸后,溶液由红色变无色,根据上述实验中颜色变化,可确定稀盐酸和氢氧化钠溶液发生了化学反应,氢氧化钠和盐酸反应生成氯化钠和水,化学反应方程式为:NaOH+HCl=NaCl+H2O;
(2)探究上述稀盐酸和氢氧化钠溶液反应后烧杯中的盐酸是否过量:
在上述设计的实验方案中,正确的是方案二,另外一个实验方案错误的原因是:氢氧化钠和盐酸反应后生成的氯化钠也能和硝酸银反应生成白色沉淀氯化银;
(3)若再设计一个确定稀盐酸是否过量的实验方案,选用的药品是锌粒,在上述溶液中加入锌粒,若有气体放出,证明稀盐酸过量,反之稀盐酸不过量。

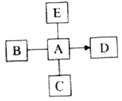
【题目】化学与生活息息相关,下列描述全部正确的一组( )
A化学与生活 | B化学与健康 |
生活中用洗洁精清洗油污的原理是乳化作用 实验室用品尝味道的方法区分食盐与白糖 | 老年人缺钙易得骨质疏松症 人体缺乏维生素A易得夜盲症 |
C化学与材料 | D化学与环境 |
塑料、天然橡胶、合成纤维都属于合成材料 玻璃钢、生铁、硬铝都属于合金 | 温室效应的形成主要与CO、CH4有关 酸雨形成主要与SO2、氮氧化合物有关 |
A. AB. BC. CD. D