题目内容
【题目】水是人类最宝贵的自然资源,依据所学化学知识回答:
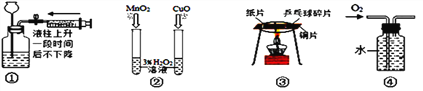
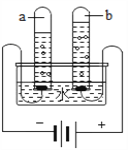
(1)利用下图所示的装置探究水的组成,通电一段时间后,试管a中收集到的气体名称是_____________。该反应的文字表达式为___________________________。若在正极得到5毫升氧气,则在负极产生______________g氢气(氢气的密度为0.0899 g/L)。
(2)鉴别一份井水是硬水还是软水,常用的物质是_________________。
【答案】 氢气 水![]() 氢气+氧气 8.99×10-4 肥皂水
氢气+氧气 8.99×10-4 肥皂水
【解析】(1)由装置可知,通电一段时间后,试管a中收集到的气体是电源的负极产生的气体较多,名称是氢气.该反应的文字符号表达式为:水![]() 氢气+氧气;若在正极得到5毫升氧气,则在负极产生10 毫升氢气,即0.01L,质量为:0.01L×0.0899g/L=8.99×10-4g;(2)鉴别一份井水是硬水还是软水,常用的物质是肥皂水,遇肥皂水产生的泡沫少的是硬水,遇肥皂水产生的泡沫多的是软水。
氢气+氧气;若在正极得到5毫升氧气,则在负极产生10 毫升氢气,即0.01L,质量为:0.01L×0.0899g/L=8.99×10-4g;(2)鉴别一份井水是硬水还是软水,常用的物质是肥皂水,遇肥皂水产生的泡沫少的是硬水,遇肥皂水产生的泡沫多的是软水。

【题目】铅蓄电池在生产、生活中使用广泛。其构造示意图如图1,回答下列问题:
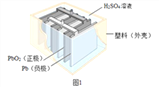
(1)图1铅蓄电池放电过程中,反应的化学方程式为 Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断_____(填“增大”、“减小”或“不变”)。
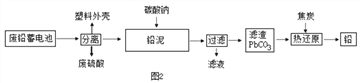
(2)如图2是回收废铅蓄电池的一种工艺流程。
①写出焦炭热还原生成铅的化学方程式: ________________________
②将流程图中的废硫酸和滤液按一定比例混合,再将所得的混合液经____、降温结晶、过滤等操作,可以析出Na2SO4·10H2O晶体。
③如表是一些金属熔点的数据:
金属 | 锡 | 铅 | 铋 | 镉 |
熔点∕℃ | 231.9 | 327.5 | 271.3 | 320.9 |
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为________________。
A. 231.9-327.5℃ B.271.3-320.9℃ C.60-80℃ D.20-40℃
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
物质 | CaCO3 | NH3 | Ca(OH)2 |
市场参考价(元/kg ) | 1.8 | 6.5 | 2.0 |
已知:2NH3+H2SO4═(NH4)2SO4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择_________ 。