题目内容
【题目】根据下表回答问题:
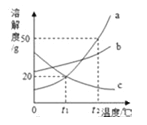
温度/℃ | 20 | 40 | 60 | |
溶解度 | NaCl | 36.0 | 36.6 | 37.3 |
| 31.6 | 63.9 | 110 | |
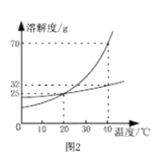
(1)60℃,100g水中最多能溶解![]() 的质量为__________。
的质量为__________。
(2)下列说法正确的是_________(填序号)。
A.20℃时,![]() 饱和溶液的质量分数为31.6%
饱和溶液的质量分数为31.6%
B.40℃时,136.6gNaCl溶液中一定含有36.6gNaCl
C.将40℃时![]() 的饱和溶液降温到20℃,析出32.3g
的饱和溶液降温到20℃,析出32.3g![]() 固体
固体
D.将40℃时NaCl和![]() 的饱和溶液分别降温至20℃,降温后两溶液质量分数的大小关系为NaCl>
的饱和溶液分别降温至20℃,降温后两溶液质量分数的大小关系为NaCl>![]()
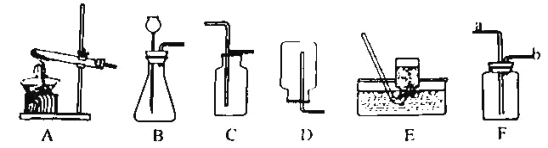
(3)20℃时,按下列图示操作:

①在溶液A、B、C中,![]() 溶解达到饱和状态的有_______(填字母)。
溶解达到饱和状态的有_______(填字母)。
②比较溶液A、B中![]() 的质量分数:A_______B(填“>“或” <”或“=”)。
的质量分数:A_______B(填“>“或” <”或“=”)。
【答案】 110g D AB >
【解析】(1)固体物质的溶解度是指在一定温度下,100g溶剂里最多能溶解的某固体物质的质量,60℃时,100g水中最多能溶解110g硝酸钾。(2)A.20℃时,![]() 的溶解度是31.6g,则KNO3饱和溶液的溶质质量分数为:
的溶解度是31.6g,则KNO3饱和溶液的溶质质量分数为:![]() ×100%≠31.6%,错误;B.40℃时,136.6gNaCl饱和溶液中一定含有36.6gNaCl,若为指明溶液的状态,则无法求算溶质的质量,错误;C.将40℃时100g溶剂所形成的
×100%≠31.6%,错误;B.40℃时,136.6gNaCl饱和溶液中一定含有36.6gNaCl,若为指明溶液的状态,则无法求算溶质的质量,错误;C.将40℃时100g溶剂所形成的![]() 饱和溶液降温到20℃,折出32.3g
饱和溶液降温到20℃,折出32.3g![]() 固体,未指明饱和溶液的质量,无法求算析出晶体的质量,错误;D.将40℃时NaCl和
固体,未指明饱和溶液的质量,无法求算析出晶体的质量,错误;D.将40℃时NaCl和![]() 的饱和溶液分别降温至20℃,溶解度都变小,由于20℃时,NaCl的溶解度大于KNO3的溶解度,所以降温后两溶液质量分数的大小关系为NaCl>
的饱和溶液分别降温至20℃,溶解度都变小,由于20℃时,NaCl的溶解度大于KNO3的溶解度,所以降温后两溶液质量分数的大小关系为NaCl>![]() ,正确。故选D。(3)①20℃时,KNO3的溶解度是31.6g,一种溶剂中可同时溶解多种溶质,且互相不影响,所以A、B是KNO3的饱和溶液。60℃时,KNO3的溶解度是110g,C是KNO3的不饱和溶液,故填AB。②一种溶剂中可同时溶解多种溶质,且互相不影响,溶液B中由于多溶解了40gNaCl,所以溶液B比溶液A的质量多40g,但两溶液中溶解KNO3的质量相等,因此溶液A、B中
,正确。故选D。(3)①20℃时,KNO3的溶解度是31.6g,一种溶剂中可同时溶解多种溶质,且互相不影响,所以A、B是KNO3的饱和溶液。60℃时,KNO3的溶解度是110g,C是KNO3的不饱和溶液,故填AB。②一种溶剂中可同时溶解多种溶质,且互相不影响,溶液B中由于多溶解了40gNaCl,所以溶液B比溶液A的质量多40g,但两溶液中溶解KNO3的质量相等,因此溶液A、B中![]() 的质量分数是:A>B。
的质量分数是:A>B。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】已知某品牌膨松剂的成分是碳酸氢钠、碳酸氢铵中的一种或两种,某化学兴趣小组为确定该品牌膨松剂的成分,进行如下探究:
查阅资料:
①氨气水溶液呈碱性
②浓硫酸和碱石灰都可做气体吸收剂;浓硫酸能吸收氨气,不能吸收二氧化碳;碱石灰是氧化钙与氢氧化钠固体的混合物,不与氨气反应。
(设计实验)兴趣小组利用如下装置进行探究(装置气密性良好,各装置中气体吸收剂足量);
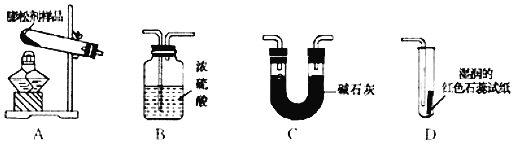
依次连接A、C、D装置,点燃A处的酒精灯,将试管中的该膨松剂样品充分加热至完全反应后,通过观察到_____、_____现象可以证明该膨松剂中含有NaHCO3和 NH4HCO3两种物质。其中装置C的作用是_____。
(拓展探究)为进一步确定该品牌膨松剂中 NaHCO3和NH4HCO3的质量比,同学们取两份等质量的该品牌膨松剂样品,利用图提供的实验装置,设计并进行了如下两组实验:
序号 | 实验操作 | 测得数据 |
实验1 | 将其中的一份膨松剂样品加入A装置试管中,将A装置依次连接B、C装置,充分加热至膨松剂完全反应 | 装置C增重1.98g |
实验2 | 将另一份膨松剂样品加人A装置试管中,将A装置依次连接C、B装置,充分加热至膨松剂完全反应 | 装置B增重0.34g |
基于以上实验数据分析,该品牌膨松剂中 NaHCO3和 NH4HCO3的质量比是_____。
(实验反思)小明认为以上拓展探究实验存在一定误差,导致误差的原因是_____(答一条即可)。