题目内容
【题目】如图,将等质量的锌 和铁分别入入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
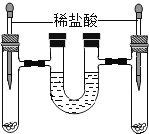
A. 右试管中溶液为黄色
B. 两试管中所得溶液的质量相等
C. U型管中液面左升右降
D. U型管中液面仍相平
【答案】D
【解析】A、铁和盐酸反应会生成氯化亚铁和氢气,氯化亚铁溶液显浅绿色,所以反应后右试管中溶液为浅绿色,错误;B、通过分析题中的反应可知,金属均有剩余,所以盐酸全部反应,生成的氢气质量相等,置换相同质量的氢气,所用的铁和锌的质量不等,所以两试管中所得溶液的质量不相等,错误;C、通过分析题中的反应可知,金属均有剩余,所以盐酸全部反应,生成的氢气质量相等,氢气的体积也相等,U形管两端的气体体积变化相等,所以U型管中液面不变,错误;D、通过分析题中的反应可知,金属均有剩余,所以盐酸全部反应,生成的氢气质量相等,氢气的体积也相等,U形管两端的气体体积变化相等,所以U型管中液面不变,正确。故选D。

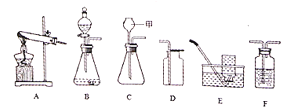
【题目】化学是一门以实验为基础的科学,请结合图示回答问题

(1)在确定实验室制取氧气的化学反应时,不需要考虑的因素是_____(填字母序号)。
a 原料中是否含有氧元素 b 原料的产地
c 实验装置是否容易装配 d 实验条件是否容易控制、实验操作是否安全可靠
(2)实验室利用大理石和稀盐酸反应制取二氧化碳,可选用图1中C、D发生装置,D与C相比优点是______________,收集二氧化碳可选择______________(填装置序号)。
(3)实验室中制取氯气,图2中H处为制备氯气的装置,应该选择图1中的______________(填装置序号);M装置的作用是______________。


(4)已知:CO2和SO2既有相似性也有差异性。请回答相关问题:
气 体 | CO2 | SO2 | |
制备 | 石灰石 | Na2SO3与70%硫酸 | |
相似性 | 溶解性 | 能溶于水 | 易溶于水 |
与澄清石灰水反应 | 二者都产生白色浑浊 | ||
差异性 | 与KMnO4溶液 | 不反应 | 气体被吸收,溶液逐渐褪色 |
①化石燃料燃烧气体产物中有CO2和SO2等物质,其中SO2是形成__________(填一污染名称)的主要物质。
②实验室制取CO2的化学方程式是_________________。
③可用Na2SO3与70%硫酸常温反应制备SO2,制备SO2的发生装置用_________________(填图装置序号)。
④将收集满SO2的试管倒扣在水中观察到的现象是_________________,SO2溶于水发生反应的化学方程式为_______________。
【题目】培养学生的科学探究能力是新课程改革的重要理念。实验室现有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),经试验员分析可知原瓶溶液中的溶质可能是NaCl、Na2OH、Na2CO3、NaHCO3中的一种。为确认其中的溶质,同学们进行了如下的探究活动。请你参与到其中去,回答有关问题。
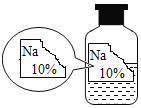
(进行猜想)猜想I:该溶液的溶质是NaCl
猜想Ⅱ:该溶液的溶质是NaOH
猜想Ⅲ:该溶液的溶质是Na2CO3
猜想IV:该溶液的溶质是NaHCO3。
(查阅资料)常温下物质的相关信息如表:
物质 | NaC1 | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
从物质的相关信息可知,该溶液的溶质不是_____,请说出理由_____。
(进行实验)
(1)测定溶液的pH大于7,该溶液的溶质不是_____。
(2)同学们又进行了如下实验,实验过程如图:
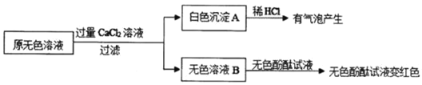
①气泡生成的化学方程式是_____。
②实验可以判断原无色溶液中含有的溶质有_____。
(获得结论)
该瓶原来装的无色溶液的溶质是NaOH,并且_____(填“没有”、“部分”或“全部”)变质。
(拓展)
若提纯该无色溶液,写出有关反应原理(用化学方程式表示)_____。