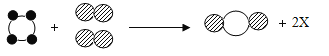
题目内容
【题目】某班同学用如图装置测定空气里氧气的含量。
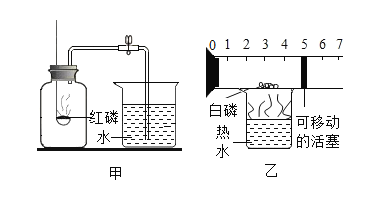
(1)甲实验中反应的化学方程式为_________________;
(2)甲实验中的红磷可换为____________________________;
A 木炭
B 蜡烛
C 白磷
D 铁丝
(3)乙中活塞的运动方向是____________________________;
(4)乙反应完毕,去掉热水,活塞最终应停留在刻度_____ 处。
(5)和甲比较,乙实验的优点是____________________________(写一点)。
【答案】4P+5O2![]() 2P2O5 C 先向右,再向左 4 反应在密闭的环境中进行,生成的五氧化二磷不会逸出污染空气
2P2O5 C 先向右,再向左 4 反应在密闭的环境中进行,生成的五氧化二磷不会逸出污染空气
【解析】
(1)红磷燃烧生成五氧化二磷,方程式为4P+5O2![]() 2P2O5,故填:4P+5O2
2P2O5,故填:4P+5O2![]() 2P2O5;
2P2O5;
(2)木炭、蜡烛燃烧会生成气体,铁丝不能在空气中燃烧,都不能代替红磷,白磷在空气中燃烧生成五氧化二磷固体,可以代替红磷,故选:C。
(3)白磷燃烧放出热量且消耗氧气,乙中活塞的运动方向是先向右,再向左运动,故填:先向右,再向左;
(4)空气中氧气占五分之一,乙反应完毕,去掉热水,活塞最终应停留在刻度4处,故填:4;
(5)和甲比较,乙实验的优点是:反应在密闭的环境中进行,生成的五氧化二磷不会逸出污染空气,故填:反应在密闭的环境中进行,生成的五氧化二磷不会逸出污染空气。

 名校课堂系列答案
名校课堂系列答案【题目】某学习小组探究气体的制备方法。
[实验可用药品探究]
(1)制取氧气时,甲同学提出,必须要用含有氧元素的物质才有可能制取氧气。他依据的原理是____ 定律
(2)工业上一般选用空气为原料制取氧气,这种方法的优点是___________________。 由于需要高压和低温条件,这种方法不适合于实验室制取氧气。
(3)下列方法中,适合实验室制取氧气的是____________;
①电解水
②加热高锰酸钾
③加热氯酸钾和二氧化锰
④用过氧化氢溶液和二氧化锰
⑤加热氧化汞
(4)[催化剂和催化作用探究]
[探究一] 影响过氧化氢分解速率的因素有哪些?小组同学做了四个实验,实验数据如下:
实验序号 | H2O2溶液的溶质质量的分数% | H2O2溶液的体积/mL | 温度/°C | MnO2的用量/g | 收集O2的体积/mL | 反应时间 |
① | 5 | 1 | 20 | 0.1 | 4 | 16s |
② | 15 | 1 | 20 | 0.1 | 4 | 6s |
③ | 30 | 5 | 35 | 0 | 4 | 98min |
④ | 30 | 5 | 55 | 0 | 4 | 20min |
③④两组实验对比可知:____________________________;
(5)能说明过氧化氢的分解速率与其质量分数有关的实验是____ ( 填实验序号)。
(6) [探究二] 其他金属氧化物能否起到类似MnO2的催化作用?实验方案如下:
I. 用MnO2、CuO、 Fe2O3、 Cr2O3 四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用下图装置进行实验。改用其他三种微球,分别重复上述实验,得到下图的锥形瓶内压强随时间变化的曲线图。
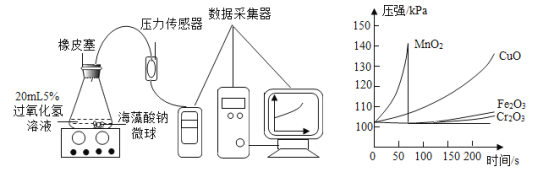
用含MnO2的海藻酸钠微球进行实验, 60 s时压强瞬间回落,其原因是______
A MnO2被反应完
B 开始实验时装置气密性不好
C 橡胶塞被气体冲出
D 数据采集器的电源被切断
(7)从实验曲线看,催化效果较好、反应温和的催化剂是____________________________。