题目内容
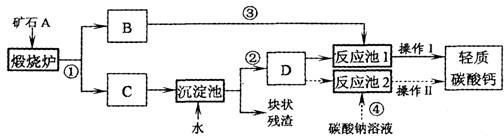
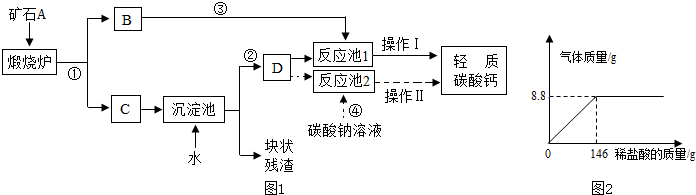
用作牙膏摩擦剂的轻质碳酸钙可以用矿石 A 来制备,某化学兴趣小组设计了 2 种转化流程,如图所示.
已知:生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆.
(1)小王主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单.请写出反应①和④的化学方程式:①
(2)制轻质碳酸钙时,D 为
(3)小李认为流程①、②、③和操作Ⅰ比小王的主张更好,其理由是

已知:生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆.
(1)小王主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单.请写出反应①和④的化学方程式:①
CaCO3═CaO+CO2↑
CaCO3═CaO+CO2↑
;④Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
; 操 作Ⅱ包 括搅拌、过滤
搅拌、过滤
等工序.(2)制轻质碳酸钙时,D 为
悬浊液
悬浊液
(选填“悬浊液”、“溶液”或“乳浊液”),理由是澄清石灰水中氢氧化钙的浓度太小,生产效率很低
澄清石灰水中氢氧化钙的浓度太小,生产效率很低
(3)小李认为流程①、②、③和操作Ⅰ比小王的主张更好,其理由是
利用产生的二氧化碳比另加碳酸钠溶液更经济,生产成本更低
利用产生的二氧化碳比另加碳酸钠溶液更经济,生产成本更低
;操作Ⅰ包括搅拌和微热等工序
分析:碳酸钙能分解生成氧化钙,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与二氧化碳或碳酸钠反应生成碳酸钙,生成的碳酸钙不溶于水,可以通过过滤的方法从溶液中分离出来.
解答:解:(1)①碳酸钙能高温分解生成氧化钙和二氧化碳,故A为碳酸钙,②生成的氧化钙与水反应生成氢氧化钙,故B为二氧化碳,C为氧化钙,生成的D为氢氧化钙,③氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,④氢氧化钙能与碳酸钠发生复分解反应生成碳酸钙和氢氧化钠,生成的碳酸钙不溶于水,可以通过过滤的方法从溶液中分离出来,故答案为:CaCO3
CaO+CO2↑,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,搅拌、过滤;
(2)轻质碳酸钙的颗粒细小,悬浊液更为合适,故答案为:悬浊液,澄清石灰水中氢氧化钙的浓度太小,生产效率很低;
(3)流程①、②、③的③是将碳酸钙分解生成的二氧化碳加以利用.故答案为:利用产生的二氧化碳比另加碳酸钠溶液更经济,生产成本更低.
| ||
(2)轻质碳酸钙的颗粒细小,悬浊液更为合适,故答案为:悬浊液,澄清石灰水中氢氧化钙的浓度太小,生产效率很低;
(3)流程①、②、③的③是将碳酸钙分解生成的二氧化碳加以利用.故答案为:利用产生的二氧化碳比另加碳酸钠溶液更经济,生产成本更低.
点评:本题考查了碳酸钙、氧化钙和氢氧化钙的相互转化,完成此题需要掌握生石灰的用途以及化学方程式的书写.

练习册系列答案
相关题目

 请回答下列问题:
请回答下列问题: