题目内容
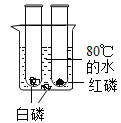
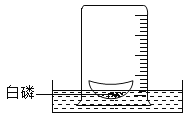
【题目】有人为了研究空气中所含氧气的体积,做了以下实验:在室温条件下,用烧杯倒扣在水中,烧杯内浮着一个不锈钢(不与白磷反应)制成的小船,船中放有少量白磷。现把浓硫酸缓缓地注入水中并搅排,放白磷的小船用不锈钢做的原因是______。不一会儿,白磷发生自燃,到反应结束并冷却后,发现烧杯内水面会上升,进入水的体积占原烧杯内空气体积的______,产生这一现象的原因是______。
【答案】不锈钢具有良好的导热性 ![]() 白磷燃烧消耗烧杯中氧气,烧杯中压强减小,水进入烧杯,进入水的体积就是氧气的体积,消耗氧气的体积约占烧杯中空气体积的
白磷燃烧消耗烧杯中氧气,烧杯中压强减小,水进入烧杯,进入水的体积就是氧气的体积,消耗氧气的体积约占烧杯中空气体积的![]()
【解析】
浓硫酸缓缓地注入水中放出热量,放白磷的小船用不锈钢做的原因是:不锈钢具有良好的导热性,以达到白磷的着火点;不一会儿,白磷发生自燃,到反应结束并冷却后,发现烧杯内水面会上升,进入水的体积占原烧杯内空气体积的![]() ;产生这一现象的原因是:白磷燃烧消耗烧杯中氧气,烧杯中压强减小,小于外界压强,水进入烧杯,进入水的体积就是氧气的体积,消耗氧气的体积约占烧杯中空气体积的
;产生这一现象的原因是:白磷燃烧消耗烧杯中氧气,烧杯中压强减小,小于外界压强,水进入烧杯,进入水的体积就是氧气的体积,消耗氧气的体积约占烧杯中空气体积的![]() 。
。

【题目】运用溶解度表与溶解度曲线回答下列问题:
温度/°C | 10 | 30 | 50 | 60 | |
溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
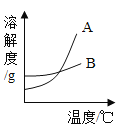
(1)B是 _____________(填“氯化钠”或“硝酸钾”)的溶解度曲线。
(2)60℃时,向100g水中加入100g硝酸钾,所得溶液的溶质质量分数为_____________,当该溶液从60℃降温到30℃时,析出晶体的质量为_____________g。
(3)现有50℃A物质的不饱和溶液,在不减少溶剂的情况下,欲使其变成饱和溶液,下列措施肯定不能实现的是_____(填序号)。
①降低温度 ②升高温度 ③加入A物质
【题目】同学们探究氢氧化钠与盐酸能否发生化学反应。
[探究活动1]同学进行了如图实验:
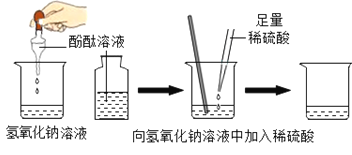
加入一定量稀盐酸后观察到溶液由红色变为无色,证明二者发生了反应。上述实验操作中有一处明显错误,请加以改正_______________。要证明稀盐酸与氢氧化钠发生了反应,除了上述方法之外,还可以按照下表实验获得结论。
实验步骤 | 实验现象 | 实验结论 |
取少量氢氧化钠溶液于试管中,加入过量稀盐酸后,再加入少量氧化铜 | ________________ | 氢氧化钠和盐酸发生了反应。加入氧化铜后发生反应的化学方程式为_____________ |
[探究活动2]如果在[探究活动1 ]中直接倾倒稀盐酸至溶液由红色变为无色,最终烧杯内的溶液中溶质的成分是什么? ( 指示剂除外)
[猜想与假设]甲猜想:氯化钠
乙猜想:_______________
甲为了证明自己的猜想,进行如下实验:
实验操作 | 实验现象 | 实验结论 |
取反应后的溶液于烧杯中,加入铁粉 | _____________ | 猜想错误 |
[探究活动3 ]中和反应能否通过判断有水生成来证明其反应发生?
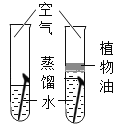
[设计实验]乙取变色硅胶、无水醋酸和氢氧化钠固体进行如图2的三个对比实验。
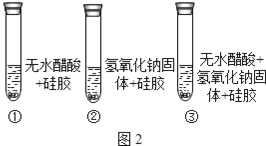
[查阅资料] a.变色硅胶吸水后由蓝色变为红色;
b.无水醋酸是一种酸,常温下为无色液体;
(1)加入试剂后.要迅速塞紧橡胶塞的原因是___________。
(2)能证明酸和碱反应有水生成的现象是___________。