题目内容
【题目】水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)“生命吸管”是一种随身携带的小型净水器,里面装有网丝,注入了活性炭和碘的树脂等,其中活性炭起到 和过滤的作用。
(2)农业上常用溶质质量分数为16%的NaCl溶液来选种,现将100g32%的NaCl溶液稀释为16%的NaCl溶液,需加水的质量为 g。
(3)请根据右图回答:
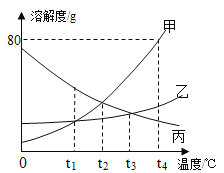
①t4℃时,将等质量的甲、乙、丙固体分别加入等质量的水中充分溶解后只得到一杯饱和溶液,该饱和溶液是 的饱和溶液;
②将丙的不饱和溶液转化为饱和溶液的方法有 。
A加丙物质 B加水 C恒温蒸发水 D升温 E降温
③将t3℃时,将等质量甲、乙、丙的饱和溶液降温至0℃时,三种溶液中溶质的质量分数由大到小的关系是 。
【答案】(1) 吸附 (2) 100 (3) ①丙② ACD③ 丙﹥乙﹥甲
【解析】
试题分析:(1) 活性炭具有疏松多孔的结构,故小型净水器,里面装有网丝,注入了活性炭和碘的树脂等,其中活性炭起到吸附和过滤的作用
(2)根据溶液稀释过程中溶质的质量不变,故可设需加水的质量为x,列式为:100g×32%=(100g+x) ×32%,x=100g
(3) ①根据溶解度曲线,t4℃时,丙的溶解度最小,故将等质量的甲、乙、丙固体分别加入等质量的水中充分溶解后只得到一杯饱和溶液,该饱和溶液是丙的饱和溶液
②根据溶解度曲线,丙的溶解度随温度的升高而降低,故将丙的不饱和溶液转化为饱和溶液,可采用的方法有:加丙物质、恒温蒸发水、升温,故选ACD
③根据溶解度曲线,物质甲、乙的溶解度都随温度的升高而增大,故将t30C时甲、乙两种物质的饱和溶液分别降温到00C时,都有晶体析出,成为00C时的饱和溶液,而在010C 时:乙的溶解度大于甲,故溶质质量分数乙也大于甲,而对于c而言,溶解度随温度的升高而降低,故t30C降温到00C,由饱和溶液变为不饱和溶液,溶液中的溶质、溶剂质量都不变,故溶质质量分数也不变,而在t30C时,物质丙的溶解度要大于00C时乙的溶解度,故丙的溶质质量分数最大,故若将t10C三种物质的饱和溶液分别升温到t20C时,则三种溶液中溶质的质量分数大小关系是:丙﹥乙﹥甲

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
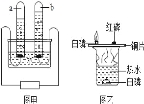
波波熊暑假作业江西人民出版社系列答案【题目】某化学兴趣小组在实验室做了如图所示的A、B两个实验。

(1)A实验中发生反应的化学方程式为: 。
(2)A、B两个实验结束后,小明同学将两支试管中的物质同时加入一纯净的烧杯中(如图C所示),混合后,观察到烧杯中有蓝色沉淀。同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究。
【猜想】
小明猜想:滤液中的溶质是Na2SO4、CuSO4;
小光猜想:滤液中的溶质是Na2SO4、NaOH;
小英猜想:滤液中的溶质是Na2SO4、CuSO4、H2SO4;
你的猜想:滤液中的溶质还可能是 。
【讨论】你认为 的猜想一定不合理,请说出理由 。
【实验】若小光的猜想正确,请完成下表的方案。
实验步骤 | 预想的实验现象 | 实验结论 |
取少量滤液于试管中,滴入 | 无色溶液变红 | 小光的猜想正确 |