题目内容
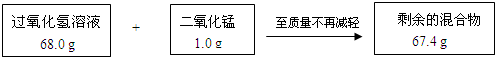
某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,实验测得相关数据如图所示:过氧化氢溶液68.0g+二氧化锰1.0g
 剩余的混合物67.4g
剩余的混合物67.4g(1)剩余的混合物中二氧化锰的质量为______g,二氧化锰在反应中的作用是______,反应生成氧气的质量为______g.
(2)计算该过氧化氢溶液中溶质的质量.
(3)计算该过氧化氢溶液中溶质质量分数.
【答案】分析:(1)二氧化锰是过氧化氢分解的催化剂,催化剂在化学反应前后质量不变;根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.因此完全反应后,物质减少的质量就是生成的气体质量;
(2)根据过氧化氢分解的化学方程式和(1)中计算出的氧气的质量,就可计算出参与反应的过氧化氢的质量;(3)根据质量分数公式计算即可.
解答:解:(1)因为催化剂在化学反应前后质量不变,故混合物中二氧化锰的质量为1.0g;根据质量守恒定律,反应生成氧气的质量=68g+1.0g-67.4g=1.6g;故答案为:1.0,催化作用 1.6
(2)设68.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2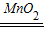 2H2O+O2↑
2H2O+O2↑
68 32
x 1.6g
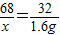
x=3.4g
答:过氧化氢溶液中溶质的质量为3.4g
(3)过氧化氢溶液的溶质的质量分数=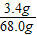 ×100%=5.0%
×100%=5.0%
答:过氧化氢溶液中溶质质量分数为5.0%
点评:本题主要考查学生根据质量守恒定律;运用化学方程式和质量分数公式进行计算的能力.
(2)根据过氧化氢分解的化学方程式和(1)中计算出的氧气的质量,就可计算出参与反应的过氧化氢的质量;(3)根据质量分数公式计算即可.
解答:解:(1)因为催化剂在化学反应前后质量不变,故混合物中二氧化锰的质量为1.0g;根据质量守恒定律,反应生成氧气的质量=68g+1.0g-67.4g=1.6g;故答案为:1.0,催化作用 1.6
(2)设68.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2
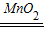 2H2O+O2↑
2H2O+O2↑68 32
x 1.6g
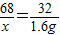
x=3.4g
答:过氧化氢溶液中溶质的质量为3.4g
(3)过氧化氢溶液的溶质的质量分数=
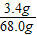 ×100%=5.0%
×100%=5.0%答:过氧化氢溶液中溶质质量分数为5.0%
点评:本题主要考查学生根据质量守恒定律;运用化学方程式和质量分数公式进行计算的能力.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目