题目内容
某化学实验小组实验结束时,将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,为回收有关金属和盐,同学们设计了如图的实验方案:
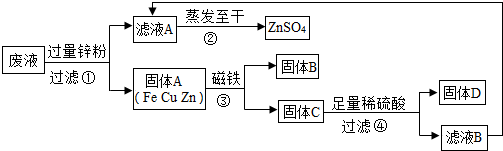
试回答:
(1)步骤①中锌粉必须过量的原因是______.
(2)写出步骤①中任一反应的化学方程式______.
(3)要检验步骤④中加入的稀硫酸是否足量的方法是______.
(4)若实验过程中的物质损失可以忽略,最终所得硫酸锌的质量______(填“>”、“<”或“=”)原废液中硫酸锌的质量.要计算该废液中硫酸铜质量,必须要称量______的质量.
解:(1)因为只有加入过量的锌才会把溶液中的铁与铜置换的更彻底一些.
故答案为:将废液中的Cu2+和Fe2+全部置换出来
(2)在此过程中发生了锌与硫酸铜和铁与硫酸铜的反应.
故答案为:Zn+CuSO4═ZnSO4+Cu(或Zn+FeSO4=Fe+ZnSO4)
(3)步骤④中的酸是否足量主要看固体D中是否含有未反应的锌,有则酸不足量,没有则酸足量.
故答案为:取步骤④的滤渣于试管中,加入少量稀硫酸,若有气泡产生,则酸不足量(或若无气泡产生,则酸已足量)
(4)因为反应过程中由于锌的加入而使其得到的硫酸锌质量变大了,由过程知铜的来源只有硫酸铜,则求硫酸铜的质量可利用得到铜的质量.
故答案为:>;固体D(或铜)
分析:(1)加入过量的锌会把溶液中的铁与铜置换的更彻底一些.
(2)步骤一中会发生两个金属与盐溶液的反应.
(3)步骤④中的酸是否足量主要看固体D中是否含有未反应的锌.
(4)得到的硫酸锌的质量应该比废液中的硫酸锌质量大,因为反应过程中由于锌的加入而使其质量变大了,要计算硫酸铜的质量可通过最后得到的铜的质量完成.
点评:此题是对物质分离知识的考查,解题时只要抓住反应过程中金属与盐溶液的反应实质,并结合相关的实验过程就能顺利解题.
故答案为:将废液中的Cu2+和Fe2+全部置换出来
(2)在此过程中发生了锌与硫酸铜和铁与硫酸铜的反应.
故答案为:Zn+CuSO4═ZnSO4+Cu(或Zn+FeSO4=Fe+ZnSO4)
(3)步骤④中的酸是否足量主要看固体D中是否含有未反应的锌,有则酸不足量,没有则酸足量.
故答案为:取步骤④的滤渣于试管中,加入少量稀硫酸,若有气泡产生,则酸不足量(或若无气泡产生,则酸已足量)
(4)因为反应过程中由于锌的加入而使其得到的硫酸锌质量变大了,由过程知铜的来源只有硫酸铜,则求硫酸铜的质量可利用得到铜的质量.
故答案为:>;固体D(或铜)
分析:(1)加入过量的锌会把溶液中的铁与铜置换的更彻底一些.
(2)步骤一中会发生两个金属与盐溶液的反应.
(3)步骤④中的酸是否足量主要看固体D中是否含有未反应的锌.
(4)得到的硫酸锌的质量应该比废液中的硫酸锌质量大,因为反应过程中由于锌的加入而使其质量变大了,要计算硫酸铜的质量可通过最后得到的铜的质量完成.
点评:此题是对物质分离知识的考查,解题时只要抓住反应过程中金属与盐溶液的反应实质,并结合相关的实验过程就能顺利解题.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
 碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
实验一:探究碳酸氢钠溶液的酸碱性
取碳酸氢钠溶液少许,滴加无色酚酞溶液变红,由此可知碳酸氢钠溶液呈______性.
实验二:探究碳酸氢钠的热稳定性
[查阅资料]碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
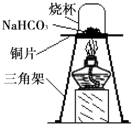
[进行实验]为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有______生成.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:______.
(3)兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3.
①兴趣小组的同学猜想的依据是______.
②请设计实验检验反应后的固体产物是NaOH还Na2CO3,并填入下表:
| 实 验 操 作 | 预期实验现象 | 结 论 |
| 取少量固体产物,向其中加入______. | 有气泡产生 | 固体产物是Na2CO3,而不是NaOH. |
 某化学兴趣小组的同学发现:发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致.发酵粉的主要成分中有碳酸氢钠(NaHCO3),俗称小苏打,他们对碳酸氢钠的性质进行了探究.
某化学兴趣小组的同学发现:发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致.发酵粉的主要成分中有碳酸氢钠(NaHCO3),俗称小苏打,他们对碳酸氢钠的性质进行了探究. 化学实验中常常会出现意外情况,这是提升我们学科素养的良好机会,要根据具体情况区别对待,善于发现和解决问题.例如:
化学实验中常常会出现意外情况,这是提升我们学科素养的良好机会,要根据具体情况区别对待,善于发现和解决问题.例如: