题目内容
【题目】工业盐酸中通常因溶有少量的 FeCl3而呈黄色,小红为测定某工业盐酸中 HCl 的含量进 行如下实验:取某工业盐酸 l00g,滴加一定溶质质量分数的 NaOH 溶液,测得加入 NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl3与 NaOH 反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题:
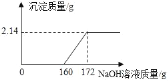
(1)FeCl3与 NaOH 恰好完全反应时,生成沉淀的质量是_____ g;
(2)所滴加的 NaOH 溶液质量为 160 克时,溶液中的溶质是_____;
(3)该工业盐酸中 HCl 的质量分数是多少?_____。
【答案】2.14g NaCl、FeCl3 29.2%
【解析】
解:(1)由图像可知,完全反应后生成沉淀的质量为2.14g;
(2)所滴加的 NaOH 溶液质量为160克时,氢氧化钠恰好与盐酸反应生成氯化钠和水,所以溶液中的溶质是生成的氯化钠和没参与反应的氯化铁;
(3)由图可知,与氯化铁反应的氢氧化钠溶液的质量为172g﹣160g=12g;
设消耗的氢氧化钠的质量为x。
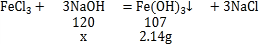
![]() ,解得x=2.4g
,解得x=2.4g
氢氧化钠溶液的溶质质量分数为:![]() ×100%=20%
×100%=20%
与盐酸反应的氢氧化钠的质量为:160g×20%=32g
设工业盐酸中HCl的质量为y。

![]()
解得y=29.2g
该工业盐酸中HCl的质量分数是:![]() ×100%=29.2%
×100%=29.2%
答:该工业盐酸中HCl的质量分数是29.2%。

练习册系列答案
相关题目