题目内容
石灰石的主要成分为CaCO3,所含杂质不溶于水,也不参加反应.某化学兴趣小组为了测定石灰石中CaCO3的质量分数,进行了以下探究实验:称石灰石样品二份,分别放入大烧杯中,第一个烧杯中加入50克稀盐酸,第二个烧杯中放入100克同样的稀盐酸,充分反应至不再有气泡产生时称量残留物质量,有关数据如下表.
求:
(1)二个烧杯中产生CO2的质量(填入上表);
(2)石灰石样品中CaCO3的质量分数.(精确到0.1%)
| 各物质的质量 | 第一个烧杯 | 第二个烧杯 |
| 石灰石样品质量 | 12g | 12g |
| 稀盐酸质量 | 50g | 100g |
| 烧杯残留物质量 | 58.7g | 107.6g |
| 产生的CO2质量 |
(1)二个烧杯中产生CO2的质量(填入上表);
(2)石灰石样品中CaCO3的质量分数.(精确到0.1%)
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据质量守恒定律可以计算出二氧化碳的质量;
(2)根据在化学方程式中二氧化碳的质量,可以计算碳酸钙的质量;
(2)根据在化学方程式中二氧化碳的质量,可以计算碳酸钙的质量;
解答:解:
(1)第一个烧杯稀盐酸完全反应,产生二氧化碳质量:12g+50g-58.7g=3.3克;
第二个烧杯石灰石样品完全反应,产生二氧化碳质量:12g+100g-107.6g=4.4克;
(2)设石灰石中CaCO3的质量为X,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
=
x═10g
石灰石中CaCO3的质量分数=
×100%=83.3%
答案:
(1)第一个烧杯产生二氧化碳质量3.3克;第二个烧杯产生二氧化碳质量4.4克
(2)石灰石样品中CaCO3的质量分数83.3%
(1)第一个烧杯稀盐酸完全反应,产生二氧化碳质量:12g+50g-58.7g=3.3克;
第二个烧杯石灰石样品完全反应,产生二氧化碳质量:12g+100g-107.6g=4.4克;
(2)设石灰石中CaCO3的质量为X,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
| 100 |
| 44 |
| x |
| 4.4g |
x═10g
石灰石中CaCO3的质量分数=
| 10g |
| 12g |
答案:
(1)第一个烧杯产生二氧化碳质量3.3克;第二个烧杯产生二氧化碳质量4.4克
(2)石灰石样品中CaCO3的质量分数83.3%
点评:本题主要考查了学生分析图表数据,解决问题的能力,以及据方程式计算的能力.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
四种物质:①空气;②液态氧;③二氧化碳;④氧化汞.其中含有氧分子的是( )
| A、①④ | B、①③ | C、①② | D、③④ |
 在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:
在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题: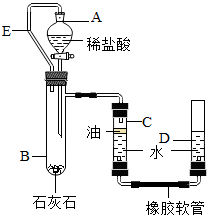 Ⅰ:金属材料用途广泛,回答下列问题:
Ⅰ:金属材料用途广泛,回答下列问题: