题目内容
 在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:
在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:(1)刚开始滴加稀硫酸没有氢气放出的原因是
(2)所滴加的稀硫酸中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)由于铝的化学性质比较活泼,易于空气中的氧气反应,在铝的表面形成了氧化铝,所以开始加入硫酸时不产生氢气;
(2)当加入9.8g稀硫酸时才产生氢气,当加稀硫酸的量至107.8g时,铝箔和硫酸恰好完全反应,产生0.2g氢气.根据铝箔和稀硫酸反应化学方程式,由氢气的质量,可求出与铝反应的硫酸中溶质的质量,再求出所滴加的稀硫酸中溶质的质量分数.
(2)当加入9.8g稀硫酸时才产生氢气,当加稀硫酸的量至107.8g时,铝箔和硫酸恰好完全反应,产生0.2g氢气.根据铝箔和稀硫酸反应化学方程式,由氢气的质量,可求出与铝反应的硫酸中溶质的质量,再求出所滴加的稀硫酸中溶质的质量分数.
解答:解:
(1)根据铝箔和稀硫酸反应化学方程式,结合题干中的右图所示知道产生氢气的质量是0.2g,刚开始滴加稀硫酸没有氢气放出的原因是:久置的铝箔表面被氧化,形成一层氧化膜.此氧化膜与硫酸反应生成硫酸铝和水,不产生氢气;
(2)由题意可知,与铝反应的硫酸的质量为:107.8g-9.8g=98g
设与铝反应的稀硫酸中溶质的质量为x.
2Al+3H2SO4═Al2(SO4)3+3H2↑
294 6
x 0.2g
=
x=9.8g
稀硫酸中溶质的质量分数为:
×100%=10%
答案:
(1)稀硫酸首先与表面的氧化铝薄膜发生了反应;
(2)所滴加的稀硫酸中溶质的质量分数10%.
(1)根据铝箔和稀硫酸反应化学方程式,结合题干中的右图所示知道产生氢气的质量是0.2g,刚开始滴加稀硫酸没有氢气放出的原因是:久置的铝箔表面被氧化,形成一层氧化膜.此氧化膜与硫酸反应生成硫酸铝和水,不产生氢气;
(2)由题意可知,与铝反应的硫酸的质量为:107.8g-9.8g=98g
设与铝反应的稀硫酸中溶质的质量为x.
2Al+3H2SO4═Al2(SO4)3+3H2↑
294 6
x 0.2g
| 294 |
| 6 |
| x |
| 0.2g |
x=9.8g
稀硫酸中溶质的质量分数为:
| 9.8g |
| 98g |
答案:
(1)稀硫酸首先与表面的氧化铝薄膜发生了反应;
(2)所滴加的稀硫酸中溶质的质量分数10%.
点评:此题考查学生会结合图示找出解题突破口,利用化学方程式进行计算,特别是解2步时,首先化学方程式要正确,再者相对分子质量要计算正确,才能解出正确的答案.请同学们考虑细致,思维要慎密.

练习册系列答案
相关题目
下列实验操作正确的是( )
A、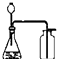 双氧水制氧气 |
B、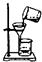 过滤液体 |
C、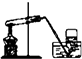 高锰酸钾制氧气 |
D、 熄灭酒精 |

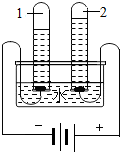 利用如图装置可以得出了水的组成,试管“1”中的气体是
利用如图装置可以得出了水的组成,试管“1”中的气体是