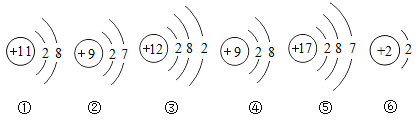
题目内容
【题目】学习了氧气的知识,兴趣小组同学对氧气在生活中的应用进行了探究。

(查阅资料)家用制氧机(如图1)的工作原理如下:加压时,装填制氧机内部的分子筛吸附空气中的氮气,制取高浓度氧气:减压时,分子筛将所吸附的氮气排放,整个过程中,分子筛并不消耗。兴趣小组同学用家用制氧机制取并收集了一袋气体,带到实验室对其进行研究。
实验一:小组同学准备通过以下实验验证所收集的气体是否为纯净的氧气。
(实验记录)取一只250mL的集气瓶,用排水法收集一瓶所带气体,然后把一根燃着的木条插入集气瓶中,木条燃烧得更旺。
(实验结论)收集的气体是纯净的氧气。
(实验反思)老师指出上述实验并不能证明小组同学所带来的气体一定是纯净的氧气。该实验不能确定所收集气体为纯净氧气的原因是___________。
实验二:测定小组同学所带气体中氧气的含量。
同学们在老师的指导下设计了如图2所示装置,进行实验,并重复多次。请补充完实验记录。
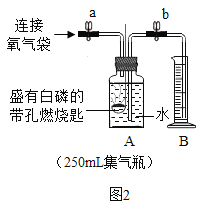
(实验步骤)
①检查____________。
②加入药品,将装置连接固定。
③打开止水夹a和b,向A中缓慢鼓入一定量气体,露出白磷后,关闭止水夹a和b, A中水进入到B中,测得B中水的体积为V1mL。
④用凸透镜聚光引燃白磷,白磷燃烧,产生大量白烟。
⑤待白磷熄灭并冷却到室温,进行_______操作。B中水倒吸进入A中,测得量筒中的体积变为V2mL 。
⑥计算小组同学所带气体中氧气的体积分数。
(1)请填(“不变”或“偏高”或“偏低”)
A 步骤③中,仰视量筒读数会使测得的V1数值____________;
B 步骤⑤中,未冷却至室温会使测得的小组同学所带气体中氧气的含量__________;
(2)(数据记录)
经测定V1=110mL; V2数据如下:
实验次序 | 1 | 2 | 3 | 4 | 5 |
B 中剩余水体积/mL | 27 | 26 | 50 | 24 | 23 |
(数据处理)
已知,在如表数据中,其中有一次数据偏差较大,存在明显误差,在数据处理时应删去。小组同学所带气体中氧气的体积分数为___________(保留小数点后一位有效数字)。
(实验反思)
①家用制氧机制氧气的过程发生的变化属于__________(填“物理变化”或“化学变化”)。
②用高锰酸钾制取氧气,由于制取成本较高,不适合大量生产,一般用于实验室制取。
③导致那次数据产生较大误差的可能原因是__________。
【答案】燃烧更旺只能说明收集气体中氧气的浓度大于空气中氧气的浓度,无法证明是纯净氧气 装置气密性 打开止水夹b 偏低 偏低 77.3% 物理 白磷不足,瓶内氧气未被消耗完
【解析】
实验一:
实验反思:
该实验不能确定所收集气体为纯净氧气的原因是燃烧更旺只能说明收集气体中氧气的浓度大于空气中氧气的浓度,无法证明是纯净氧气。
实验二:
实验步骤:
①连接好仪器,先检查装置气密性。
⑤待白磷熄灭并冷却到室温,进行打开止水夹b操作,B中水倒吸进入A中,测得量筒中的体积变为V2mL。
(1) A. 步骤③中,仰视量筒读数会使测得的V1数值偏低;
B. 步骤⑤中,未冷却至室温会使进入集气瓶中的水偏少,使测得的小组同学所带气体中氧气的含量偏低;
(2) 数据处理:
已知,在如表数据中,其中第三次的数据偏差较大,存在明显误差,在数据处理时应删去,则:B中剩余水体积为:(27mL+26mL+24mL+23mL)÷4=25mL,小组同学所带气体中氧气的体积分数为:![]() .
.
实验反思:
①家用制氧机制氧气的过程没有新物质生成,发生的变化属于物理变化。
③导致第三次数据产生较大误差的可能原因是白磷不足,瓶内氧气未被消耗完。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】催化剂在生产、生活和科研中的地位越来越重要。
探究一:验证MnO2在过氧化氢分解前后的质量没有改变。
某同学用电子天平称取1.0gMnO2于试管中,加入适量过氧化氢溶液,写出发生反应的化学方程式_____________。反应结束后,过滤、洗涤、称量,发现所得固体质量大于1.0g,其可能原因是____________。小强针对上述原因提出烘干后再称量的方案,结果得到了准确的实验结果。
探究二:温度对过氧化氢反应速率的影响。
某同学用如图所示装置进行实验,发现加热后产生气泡速率明显加快,但用带火星的木条检验产生的氧气时,木条很难复燃,其可能原因是____________。
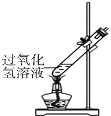
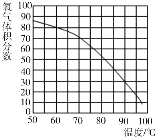
经实验测定,受热液体的温度与得到氧气的体积分数之间存在一定关系(如图所示)。若能使带火星木条复燃所需氧气的体积分数最低为49%(只考虑氧气的体积分数对实验结果的影响),现欲使带火星的木条复燃,应将加热过氧化氢溶液的最高温度控制在_________ ℃以下。
探究三:红砖粉是否也能作过氧化氢分解的催化剂?效果怎样?
小雨以收集等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
编号 | 过氧化氢 | 其他物质 | 待测数据 |
实验1 | 20mL 5% 过氧化氢溶液 | 无 | |
实验2 | 20mL 5% 过氧化氢溶液 | 1g红砖粉 | |
实验3 | 20mL 5% 过氧化氢溶液 | 1g二氧化锰 |
(1)上表中的“待测数据”是_____________。
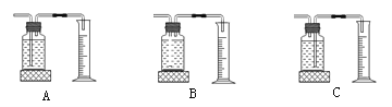
(2)如图可用于此实验收集O2的装置是_________(填字母)。一开始导管排出的气体是否收集?其理由是____________。
(3)通过实验1与实验____________的待测数据对比,可说明红砖粉能改变过氧化氢分解速率。
(4)如需证明红砖粉可作过氧化氢分解的催化剂,还需通过实验证明_______。
【题目】学习了二氧化锰对过氧化氢有催化作用的知识后。某同学想:氧化铜能否起到类似二氧化锰的催化剂作用呢?于是进行了如下探究。
(猜想)Ⅰ氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ氧化铜是反应的催化剂,反应前后_______________和_____________不变。
(实验)用天平称量![]() 氧化铜,取
氧化铜,取![]() 的过氧化氢溶液于试管中,进行如下实验:
的过氧化氢溶液于试管中,进行如下实验:
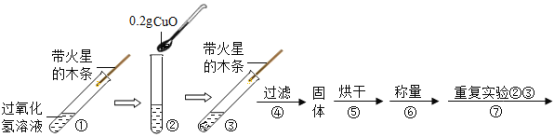
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
①_____________ ②带火星的木条复燃 | 所得固体_________g | 溶液中有气泡放出 ②带火星的木条______(填“复燃”或“不复燃”) | 猜想Ⅰ、Ⅱ不成立猜想Ⅲ成立 |
(2)步骤①的目的是___________________。
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的文字表达式为:___________________。
(4)过氧化氢反应生成氧气的快慢除了与是否使用催化剂有关,与催化剂的种类有关外,还与什么因素有关呢?请写出你的猜想并设计实验方案验证你的猜想。
①你的猜想是过氧化氢反应生成氧气的快慢与_________________有关;
②你的实验方案是:____________________。
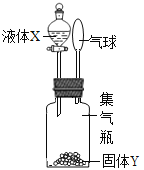
【题目】如图所示,将液体X加入到集气瓶中与固体Y作用,观察到气球逐渐变大,如表中液体X和固体Y的组合,符合题意的是( )
① | ② | ③ | ④ | ⑤ | |
X | 稀盐酸 | 水 | 水 | 双氧水 | 水 |
Y | 铁粉 | 氢氧化钠 | 氯化钠 | 二氧化锰 | 硝酸铵 |
A. ①②⑤ B. ①③④ C. ①②④ D. ②③⑤