题目内容
【题目】实验室常用过氧化氢溶液与二氧化锰混合制取氧气。现将3克二氧化锰放入盛有100克过氧化氢溶液的锥形瓶中,反应结束后,锥形瓶中物质的总质量为101.4克。请完成下列问题:
(1)反应结束后,共收集到氧气的质量为多少克?
(2)计算参加反应的过氧化氢的质量。
(3)反应结束后所得101.4克物质中含有那些物质?质量分别是多少?
【答案】(1)1.6g(2)3.4g(3)MnO2、水;3g、98.4g
【解析】
(1)根据质量守恒定律可得,生成的氧气的质量=3g+100g-101.4g=1.6g;
(2)设:参加反应的过氧化氢的质量为x。
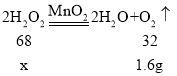
![]() x=3.4g;
x=3.4g;
(3)由于二氧化锰为催化剂,所以过程中质量不变,仍为3g,所以水的质量=101.4g-3g=98.4g。
答:(1)反应结束后,共收集到氧气的质量为1.6克;
(2)参加反应的过氧化氢的质量为3.4g;
(3)反应结束后所得101.4克物质中含有二氧化锰3g,水98.4g。

 超能学典应用题题卡系列答案
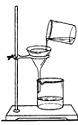
超能学典应用题题卡系列答案【题目】﹤1﹥根据如图所示的部分实验装置,回答有关问题
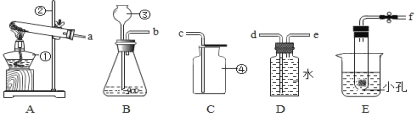
(1)写出图中仪器④的名称是_________。
(2)实验室常用装置A制O2,写出反应容器中产生O2 的化学方程式 _________ ;如用装置 D 进行收集,则应将导管 a 端与导管_____端相连。小明在帮老师整理实验室时,发现一瓶未密封的KOH固体,对其成分提出以下假设,并在老师的指导下进行实验探究。
(查阅资料):①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是____。
② K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性。
(猜想假设):假设I:只含KOH; 假设Ⅱ:含KOH和K2CO3; 假设Ⅲ:只含K2CO3
(进行实验):
实验操作步骤 | 实验现象 | 实验结论 |
① 取少量样品于试管中,加入足量的稀盐酸 | 有气泡产生 | 假设_____不正确 |
② 另取少量样品于试管中,加水溶解,加入过量的BaCl2溶液,振荡,静置 | ____ | 假设Ⅲ正确 |
③ 取②中上层清液,滴加无色酚酞溶液 | _____ |
(问题讨论):步骤②中加入过量BaCl2溶液的作用是________。
(拓展应用):完全变质的KOH也有利用价值,从K2CO3的组成或性质看,这瓶变质的试剂在农业上的用途是_________。